已知: ① 2FeCl3 + 2KI ="=" 2FeCl2 + 2KCl + I2, ② 2FeCl2+Cl2 ="==" 2FeCl3
根据①②两式判断各物质的氧化性由强到弱的顺序 。
| A.FeCl3 > Cl2 > I2 | B.Cl2 > FeCl3 > I2 | C.I2> Cl2 > FeCl3 | D.Cl2> I2> FeCl3 |
某元素的同位素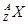 ,它的氯化物XCl2 2.22g溶于水制成溶液后,加入2mol/L的
,它的氯化物XCl2 2.22g溶于水制成溶液后,加入2mol/L的
AgNO3溶液20ml恰好完全反应,若这种同位素原子核内有20个中子,求:
(1)A=
(2)X元素在周期表中的位置?,XCl2的化学式:。
有A,B,C,D,E五种短周期元素,A与B可形成BA型化合物,且A元素是非金属性最强的元素.金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8个;C元素有三种同位素C1,C2,C3,自然界里含最多的是C1,C3的质量数是C1的3倍,C2的原子的质量数是C1的2倍.D的气态氢化物的水溶液呈碱性,而其最高价氧化物的水化物为强酸,E元素原子的最外层电子数比次外层电子数多4个,E离子的核外电子数比质子数多2个.
(1)写出元素名称:A.B.C.D.E..
(2)写出C1,C2, C3粒子的符号:,,
(3)写出E离子的结构示意图E的氢化物的分子式.
(4)写出A的单质与B的单质反应的化学方程式;
(5)写出A的单质和B的单质分别与水反应的化学方程式,,将二者反应后生成的溶液混合,发生反应的离子方程式为
(6)A与C形成的化合物中含化学键类型是.用电子式表示该化合物的形成过程.
(1)根据NaH的存在,有人提议可把氢元素放在族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的族。
(2)现有甲、乙两种元素,甲元素在第三周期第VIIA族,甲元素与碘元素相比较,非金属性较强的是(填元素名称),写出可以验证该结论的一个化学反应方程式
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。甲、乙两元素相比较,金属性较强的是(填名称),可以验证该结论的实验是()。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
X、Y、Z、W是中学化学中常见的四种气体。已知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是化石燃料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业的汽车尾气中的有害物质之一,能与水反应;W气体的水溶液滴入酚酞变红色。
请回答下列问题:
(1)X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为;
(2)科学家发现,Z在催化剂条件下能与W反应生成无毒物质,化学方程式为;其中的氧化剂是(填化学式)。
(3)在Z与水的反应中,氧化剂与还原剂的物质的量之比为。
(4)检验W气体的方法是。
(1)写出下列物质在水溶液中的电离方程式
氯化铜
硫酸铁
(2)写出下列反应的离子方程式
硫酸溶液与氢氧化钡溶液混合
碳酸氢钠溶液与稀盐酸混合