在密闭容器中进行如下反应:A(s)+2B(g) 3C(g) △H<0,达平衡后,改变下列反应条件,相关叙述正确的是
3C(g) △H<0,达平衡后,改变下列反应条件,相关叙述正确的是
| A.加入少量A,正反应速率增大,平衡向正反应方向移动 |
| B.降低温度,正反应速率加大,逆反应速率变小,平衡向正反应方向移动 |
| C.增大压强,正反应速率和逆反应速率都增大,平衡向逆反应方向移动 |
| D.增大压强,能加快反应速率的主要原因是增大了活化分子的百分数 |
下列说法正确的是
| A.盛装NaOH溶液的试剂瓶用橡胶塞,不用玻璃塞 |
| B.水晶是无色透明的晶体,可以制成硅太阳能电池 |
| C.将FeCl3饱和溶液滴入沸水中,可以立即得到Fe(OH)3胶体 |
| D.不能通过丁达尔效应来鉴别Fe(OH)3胶体和CuSO4溶液 |
下面有关碳酸钠和碳酸氢钠说法不正确的是
| A.碳酸氢钠不稳定,受热易分解 |
| B.碳酸氢钠可以用作治疗胃酸过多的药物 |
| C.碳酸钠溶液显碱性,所以碳酸钠是碱 |
| D.碳酸钠既是钠盐、又是碳酸盐、还是可溶性盐 |
某些试剂瓶上常贴有危险化学品的标志。盛装浓硫酸的试剂瓶上所贴标志应该是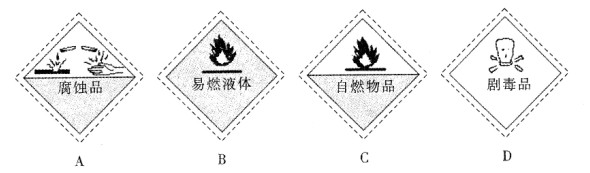
ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒。
(1)消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,此过程说明ClO2具有(填“氧化”或“还原”)性。
(2)工业上可以通过下列方法制取ClO2,请完成该反应化学方程式:2KClO3+SO2=2C1O2+ 。
实验室欲配制100 mL、1mol/L的NaCl溶液,请回答:
(1)不需要使用的仪器是。
A、烧杯B、500 mL容量瓶C、量筒 D、胶头滴管 E、玻璃棒 F、100 mL容量瓶
(2)配制时用托盘天平应称取NaClg。
(3)配制溶液的操作顺序是(用字母表示) 。
A、称量 B、洗涤 C、定容 D、溶解 E、摇匀 F、转移