著名化学家徐光宪,因为在稀土萃取领域取得了卓越成就而获得“国家最高科学技术奖”,被誉为“稀土界的袁隆平”。已知:稀土金属铈(Ce)在空气中易氧化变暗,受热时燃烧,遇水很快反应。(注:铈常见的化合价为+3和+4;氧化性:Ce4+>Fe3+。)下列说法正确的是
A.四种核素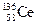 、 、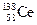 、 、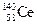 、 、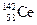 ,它们互称为同素异形体 ,它们互称为同素异形体 |
| B.铈溶于氢碘酸的化学方程式可表示为:Ce + 4HI ="==" CeI4 + 2H2↑ |
| C.在一定条件下,电解熔融状态的CeO2制Ce,在阴极获得铈 |
| D.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4+ + 2Fe2+ ="==" Ce3+ + 2Fe3+ |
下列基态原子的电子排布式中,其未成对电子数最多的是
| A.1s22s22p63s23p63d64s2 | B.1s22s22p63s23p64s1 |
| C.1s22s22p63s23p63d54s1 | D.1s22s22p63s23p63d104s1 |
下列电子式中错误的是
| A.Mg2+ | B.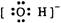 |
C.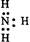 |
D.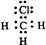 |
14C是一种放射性同位素,在高层大气中由宇宙射线产生的中子或核爆炸产生的中子轰击14N可使它转变为14C。下列说法正确的是
A.14N核外电子数与中子数相同B.14C的核外电子数为8
C.14C和14N互为同位素D.14C和12C的所有性质都相同
将2.32g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1 mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如下图所示,下列说法中错误的是
| A.OA段发生反应的离子方程式为:H++OH-===H2O CO32-+H+===HCO3- |
| B.当加入35mL盐酸时,产生CO2的体积为224mL |
| C.A点溶液中的溶质为NaC1、NaHCO3 |
| D.混合物中NaOH的质量0.60g |
向一定量的Cu、Fe2O3的混合物中加入100 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为
| A.3.2 g | B.2.4 g | C.1.6 g | D.0.8 g |