下图是部分常见元素的单质及其化合物的转化关系图(有关反应的条件及生成的部分产物已略去)。已知:E为红棕色固体,K为浅绿色溶液;反应①②是化工生产中的重要反应;B、C、D、H是单 质;B、C、D、F、G、H常温下是气态; F和H的水溶液均具有漂白作用,且F是形成酸雨的主要物质之一;N是一种常见的氮肥;化合物G为极易溶于水且易液化.
质;B、C、D、F、G、H常温下是气态; F和H的水溶液均具有漂白作用,且F是形成酸雨的主要物质之一;N是一种常见的氮肥;化合物G为极易溶于水且易液化.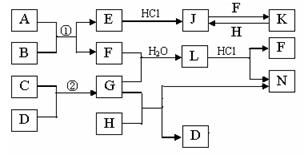
(1)化合物A中含有的短周期元素是 (写元素符号),E的化学式_______。
(2)如何检验化合物N中的阳离子 。
(3)写出J与F反应的离子方程式: ,G与H反应的化学方程式: 。
(4)等物质的量F和H的混合气体通入品红溶液中的现象为 ,原因是(用化学反应方程式表示) 。
(5)已知C与D反应生成1.7g G 时放出4.26kJ的热量,则该反应的热化学方程为
。
A、B、C、X均为中学化学中常见的纯净物,它们之间有如图所示的转化关系(副产物已略去)。
试回答:
(1)若X是强氧化性单质,则A可能是。(填序号)
a、S b、Na c、Mg d、Al
(2)若X为金属单质,向C的溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为;C溶液在储存时应加入少量X,理由是(用离子方程式表示)。
(3)若A、B、C为含同种金属元素的无机化合物,X为强酸或强碱。A和C在H2O溶液中反应生成B的离子方程式为。
X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条
件:①元素周期表中,Z与Y相邻,Z与W相邻;②X分别与Y、Z、W可组成化学式为YX3、X2Z和X2W三种共价化合物。请填空:
(1)X、Y、Z原子最外层电子数之和是;
(2)X2W的电子式是 ,YX3、X2Z和X2W形成的晶体类型都属于;
(3)X、Y和Z组成的一种化合物是强酸。写出该酸的稀溶液与铜反应的离子方程式;X、Y和Z组成的另一种化合物是离子化合物,该离子化合物在210℃分解生成一种只含Y、Z的气体和一种只含X、Z的液体(在常温、常压下)。已知40g该离子化合物完全分解可生成11.2L的气体(标准状况下),该气体的化学式为:;
(4)X、Y、Z和W组成一种化合物,其原子个数之比为5:1:3:1;该化合物具有还原性。
①写出该化合物与过量稀NaOH溶液反应的离子方程式:。
②请设计实验证明该化合物具有还原性:
。
(1)某学生在实验室做了5个实验
①在铝盐溶液中逐滴加入稀氨水直至过量,
②在明矾溶液中加入NaOH溶液直至过量,
③在强碱性溶液中逐滴加入铝盐溶液直至过量,
④在偏铝酸钠溶液中通入CO2直至过量,
⑤在强酸溶液中逐滴加入偏铝酸钠溶液直至过量。
并根据以上实验画出下列5种图象(纵坐标为沉淀的物质的量,横坐标为溶液中加入物质的量)实验与图象对应关系正确的是:___________。
| A.①和(a) | B.②和(b) | C.③和(e) | D.④和(c) |

(2)已知:氧化性:KMnO4>HNO3;Bi位于周期表中VA,+3价较稳定,NaBiO3溶液为无色。取一定量的Mn(NO3)2溶液依次进行下列实验,现象记录如下。
①滴加适量的NaBiO3溶液,溶液变为紫红色。
②继续滴加适量H2O2,紫红色褪去,并有气泡产生。
③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
④最后通入足量的SO2气体,
请回答下列问题:
(a)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为__________________________;
(b)实验④中的现象为:______________________________;
(c)实验②③反应的离子方程式分别是:
____________、______。
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。
⑴图中的两处明显的错误是
_____________________________________。
_____________________________________。
⑵A仪器的名称是___________,
B仪器的名称是。
⑶实验时A中除加入少量自来水外,还需加入少量,
其作用是_____。
对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、洗气、加热分解等。下列各组混和物的分离或提纯应采用什么方法?
①实验室中的石灰水久置,液面上常悬浮有块状CaCO3。可用 的方法除去Ca(OH)2溶液中悬浮的CaCO3。
②除去H2中的CO2,可用的方法除去。
③除去乙醇中溶解的微量食盐可采用的方法。
④粗盐中含有不溶性的泥沙、可溶性的氯化钙、氯化镁及一些硫酸盐。要将粗盐提纯,可先将粗盐溶解,按一定的顺序加入沉淀剂,再;然后将滤液调成中性并就可以得到纯净的氯化钠。
⑤除去氧化钙中的碳酸钙可用的方法。