下列叙述错误的是
| A.烧碱和消石灰都是碱 |
| B.金属与盐溶液的反应都是置换反应 |
| C.钢是用量最大、用途最广的合金 |
| D.金属钾、钠、及钾钠合金的熔点关系:钠>钾>钾钠合金 |
用下列实验装置进行相应实验,能达到实验目的的是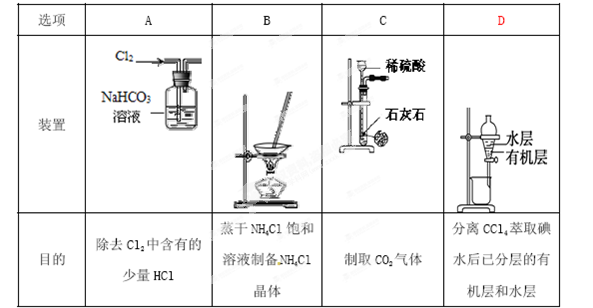
下列各组中的两种物质相互反应时,无论哪种过量,都可用同一个离子方程式表示的是
①氯气与铁粉反应②碳酸氢钠溶液与盐酸③硫酸铁溶液与氨水④氯化铁溶液与硫化钠溶液
⑤碘化亚铁溶液与氯水⑥碳酸氢钙溶液与澄清石灰水
| A.②③⑥ | B.①③⑥ | C.①②④ | D.③⑥ |
设NA为阿伏加德罗常数的值,下列叙述正确的
| A.50 mL 12 mol•L-1 浓盐酸与足量二氧化锰加热反应,转移电子数为0.3 NA |
| B.5.6 g 铁与0.1 mol 氯气充分反应转移电子数为0.3NA |
| C.1L1mol·L-1NaClO 溶液中含有ClO-的数目为NA |
| D.60gSiO2晶体中含有硅氧键的数目为4 NA |
Na2O2、HCl、Na2SO3三种物质在水中完全反应后,溶液恰好呈中性,且反应过程中无气体放出,则Na2O2、HCl、Na2SO3的物质的量之比可能为
| A.2︰3︰2 | B.1︰2︰1 |
| C.2︰3︰1 | D.4︰2︰1 |
下列离子方程式中,正确的是
| A.已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO 溶液中通入少量二氧化碳:ClO-+CO2+ H2O =HClO+HCO3- |
| B.碳酸氢钠溶液与醋酸溶液混合: CO32-+ 2H+ = H2O+ CO2↑ |
| C.从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
| D.FeCl2溶液中滴加NaClO 溶液生成红褐色沉淀:2Fe2+ + ClO-+ 5H2O= 2Fe(OH) 3↓+Cl-+ 4H+ |