下列说法正确的是 ( )
| A.在101 kPa、25 ℃时,中和热为57.3 kJ/mol,则表示Ba(OH)2的稀溶液与足量稀硫酸反应的热化学方程式为: Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l) ΔH=-114.6 kJ/mol |
| B.在101 kPa、25 ℃时,2 g H2完全燃烧生成液态水,放出285.8 kJ的热量;则氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=-285.8 kJ/mol |
| C.pH=11的氨水和pH=3的盐酸等体积混合,由于NH4Cl水解而使溶液呈酸性 |
| D.在相同情况下,强电解质溶液的导电性比相同浓度弱电解质溶液的导电性强 |
下列醇既能被催化氧化生成醛,又能发生消去反应生成烯烃的是
| A.CH3OH | B. |
C.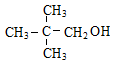 |
D. |
下列关于反应热的说法正确的是
| A.当△H<0时,表示该反应为吸热反应 |
| B.放热反应可以自发进行,而吸热反应需加热才能进行 |
| C.1molCH4完全燃烧生成CO2和水蒸气放出的热量大于生成CO2和液态水放出的热量 |
| D.化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 |
下列关于金属腐蚀与防护的说法正确的是
| A.古代青铜文物在干燥环境中的腐蚀比潮湿环境中快 |
| B.当镀锌铁制品的镀层破损时,镀层不能对铁制品起保护作用 |
| C.将钢闸门与直流电源的正极相连可防止其被腐蚀 |
| D.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
下列选项中的反应类型与其他三个选项反应类型不同的是
A.CH2 = CH2+H2O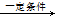 CH3CH2OH CH3CH2OH |
B.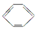 +HNO3 +HNO3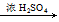 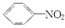 +H2O +H2O |
C.CH3COOH+CH3CH2OH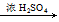 CH3COOCH2CH3+H2O CH3COOCH2CH3+H2O |
| D.CH3COOH+Cl2 → ClCH2COOH+HCl |
下列反应只能生成一种有机物的是
| A.乙烷与氯气发生取代反应 | B.CH3-CH=CH2与HCl发生加成反应 |
C. 发生消去反应 发生消去反应 |
D.CH3CH2CH2Cl与水发生取代反应 |