在一个容积固定的密闭容器中,发生反应:CO(g)+2H2(g)  CH3OH(g);ΔH<0。第2 min时只改变一个条件,反应情况如下表:
CH3OH(g);ΔH<0。第2 min时只改变一个条件,反应情况如下表:
| 时间 |
c(CO)/ mol/L |
c(H2)/mol/L |
c(CH3OH)/ mol/L |
| 起始 |
1 |
3 |
0 |
| 第2 min |
0.8 |
2.6 |
0.2 |
| 第4 min |
0.4 |
1.8 |
0.6 |
| 第6 min |
0.4 |
1.8 |
0.6 |
下列说法不正确的是
| A.第4 min至第6 min该化学反应处于平衡状态 |
| B.第2 min时,如果只改变某一条件,则改变的条件可能是降低温度 |
| C.第2 min时,如果只改变某一条件,则改变的条件可能是使用催化剂 |
| D.第6 min时,其他条件不变,如果升高温度,正反应速率增大 |
化工厂常用浓氨水检验管道是否漏氯气,反应的化学方程式为:3Cl2+8NH3====6NH4Cl+N2,当有10.65 g Cl2消耗时,被氧化的氨的质量为()
| A.3.4 g | B.1.7 g | C.6.8 g | D.0.85 g |
某CaCl2样品中可能混有FeCl3、MgCl2、NaCl、Na2CO3中的一种或两种杂质,取11.1 g样品溶解,得无色溶液,再加入足量的AgNO3溶液得29.7 g沉淀,由此可知,样品所含杂质的正确结论是()
| A.一定无Na2CO3,可能有MgCl2 | B.一定有FeCl3,可能有NaCl |
| C.一定有MgCl2,可能有NaCl | D.一定有NaCl |
现有KCl和KBr的混合物3.87 g,将混合物全部溶于水,并加入过量的AgNO3溶液,充分反应后产生6.63 g沉淀物,则原混合物中钾元素的质量分数为()
| A.24.1% | B.25.9% | C.40.3% | D.48.1% |
下列离子方程式书写正确的是()
| A.氯气和水的反应:Cl2+H2O====2H++Cl-+ClO- |
B.向漂白粉溶液中通入过量的二氧化碳:ClO-+CO2+H2O====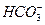 +HClO +HClO |
| C.二氧化锰与浓盐酸反应:MnO2+4HCl====Mn2++2Cl-+Cl2↑+2H2O |
| D.溴化钠与氯水反应:Br-+Cl2====Br2+Cl- |
碘元素有多种价态,可以形成多种含氧阴离子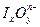 。由2个I
。由2个I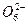 正八面体共用一个面形成的
正八面体共用一个面形成的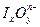 的化学式为()
的化学式为()
A.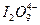 |
B.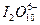 |
C.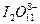 |
D.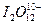 |