用48 mL 0.1 mol/L的FeSO4溶液,恰好还原2.4×10-3 mol[RO(OH)2]+离子,则R元素的最终价态为
| A.+1 | B.+2 | C.+3 | D.+4 |
下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是
① 过滤② 蒸发③ 溶解④ 向容量瓶转移液体
| A.①和② | B.①和③ | C.③和④ | D.①和④ |
一些装有化学物质的容器上常贴有危险化学品的标志。下列标志中,应贴在装有浓硫酸的容器上的是
在1 L含0.1 mol NaAlO2和0.1 mol Ba(OH)2的混合溶液中,逐滴加入浓度为0.1 mol/L的H2SO4溶液,下列图象中能表示反应产生沉淀的物质的量与加入硫酸溶液体积之间关系的是()
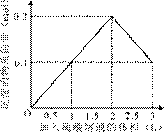
A B

C D
在标准状况下,三个干燥的烧瓶内分别装入:干燥纯净的NH3、含有部分空气的HCl气体、体积比为4:10的NO2与O2的混合气体。分别做喷泉实验,最终三个烧瓶中所得溶液的物质的量浓度(假设溶液不外渗)之比为()
| A.2:1:2 | B.5:5:4 | C.1:1 :1 :1 |
D.4:4:5 |
将充有amLNO和bmLNO2的试管倒立于水槽中,然后再通入amLO2,若a<b,则充分反应后,试管内剩余气体的体积是()
A.(a+ |
B. |
C. |
D. |