某温度下在2L密闭容器中,反应2SO2+O2 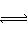 2SO3进行一段时间后SO3的物质的量增加了0.4 mol ,在这段时间内用O2表示的反应速率为0.4 mol·L-1·s-1,则这段时间为( )
2SO3进行一段时间后SO3的物质的量增加了0.4 mol ,在这段时间内用O2表示的反应速率为0.4 mol·L-1·s-1,则这段时间为( )
| A.0.1s | B.0.25s | C.0.5s | D.2.5s |
将0.1 mol N2和0.3 mol H2置于密闭容器中发生反应:N2+3H2 2NH3,下列关于该反应的说法中正确的是
2NH3,下列关于该反应的说法中正确的是
| A.增大压强,反应速率减小 |
| B.最终可生成0.2 mol NH3 |
| C.升髙温度,反应速率增大 |
| D.当V正(N2):V 正(H2)=1:3时,一定达化学平衡状态 |
在一定温度下,反应A2(g)+B2(g) 2AB(g)达到反应限度的标志是
2AB(g)达到反应限度的标志是
A.A2、B2和AB共存
B.A2、B2和AB的物质的量不再改变
C.c(A2):c(B2):c(AB)=1 :1 :2
D.A2和B2的物质的量之和与AB的物质的量相等
在一个0.5L密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-1和5.4 mol·L-1,在一定的条件下发生反应N2(g) + 3H2(g) 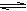 2NH3(g)。10min后测得N2的浓度是0.8 mol·L-1,则在这10min内NH3的平均反应速率是
2NH3(g)。10min后测得N2的浓度是0.8 mol·L-1,则在这10min内NH3的平均反应速率是
| A.0.1mol·L-1·min-1 | B.0.6mol·L-1·min-1 |
| C.0.3mol·L-1·min-1 | D.0.2mol·L-1·min-1 |
实验室用3.0 mol·L-1的硫酸溶液与锌粒反应制取氢气。下列措施中可能加大反应速率的是
| A.适当降低温度 | B.将锌粒改为锌粉 |
| C.将所用硫酸换成98%的浓硫酸 | D.加入少量醋酸钠固体 |
影响化学反应速率的因素很多,下列措施肯定不能加快化学反应速率的是
| A.降低温度 | B.升高温度 | C.使用催化剂 | D.增加反应物浓度 |