市场上销售的咸菜干酱牛肉咸水鸭都食品都采用真空包装,目的是为了除去空气,使大多数微生物因缺少而停止繁殖,同时防止食品发生而变质。还可以充入某种保护气来延长食品的保质期,例如薯条等小食品充入气。
现有①蜡烛、②红磷、③硫、④木炭、⑤铁丝五种物质分别在氧气中燃烧,请用序号填空:
(1)发出明亮的蓝紫色火焰的是;
(2)产生的气体能使澄清的石灰水变浑浊的是;
(3)产生大量白烟的;
(4)生成的气体会污染空气 的;
(5)属于氧化反应但不属于化合反应的。
(6)火星四射的是。
下面是实验室制取氧气的装置图,根据装置图回答下列问题: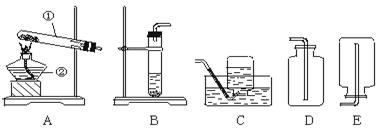
(1)写出装置图中标有①②序号的仪器名称:① ②________
(2)实验室用高锰酸钾制取氧气时,可选用的发生装置代号,该装置一个明显错误是,其目的是;可选用的收集装置是 或(写出装置代号)。
(3)用高锰酸钾制取氧气反应的文字表达式为。
(4)填写检验该气体是氧气的实验报告:
| 操作方法 |
实验现象 |
结论 |
| 是氧气 |
(5)该实验制取氧气与用氯酸钾和二氧化锰混合制取氧气操作步骤相同,实验前都应该先。实验结束时应先,后。目的是。
(6)某同学选用氯酸钾制取氧气,发现实验室没有二氧化锰,于是就加入少许高锰酸钾,也能加快反应速率。高锰酸钾是不是该反应的催化剂?(填“是”或“不是”) ,理由是。能加快反应速率的原因是。
目前有些人热衷于利用高压氧舱、氧吧、氧气袋等进行吸氧,以增加大脑供氧量,消除脑疲劳。医生建议吸氧要适量.因为高浓度的氧气往往会对人造成伤害,引起氧中毒。
(1)氧气的化学性质比较活泼,具有氧化性。它能将人体内的有机物氧化分解成二氧化碳和水,同时释放出供生命活动所需,该变化属于变化(填“物理”或“化学”)。
(2)我们有很多方法可以制取氧气,例如用过氧化氢与二氧化锰混合,该反应的文字表达式为:,该反应的基本反应类型属于反应,二氧化锰在反应中起作用。
阅读以下有关“空气成分”卡通图,填空并把你从图中获得的信息填在横线上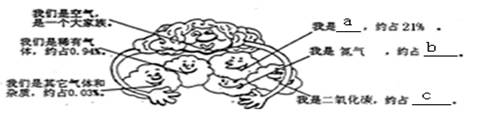
1. 填写下列序号中的结论: a;b;c 。
2.你还能得到的其他信息是:(1);
(2)。