CH3COONa稀溶液中分别加入少量下列物质或改变如下条件,能使比值
c (CH3COO-)/ c (Na+) 一定减小的是:
①固体NaOH ②固体KOH ③固体NaHSO4 ④固体CH3COONa ⑤冰醋酸 ⑥降温
| A.只有①③ | B.①③④ |
| C.②④⑤⑥ | D.③④⑥ |
下列关于化学用语的表示正确的是
A.碘化铵的电子式: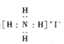 |
B.间二甲苯的结构简式: |
C.中子数为146、质子数为92的铀(u)原子: |
D.氯原子的结构示意图: 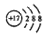 |
下列关于物质分类的说法正确的是
| A.醋酸、氨水、硫酸钡均属于弱电解质 |
| B.铜合金、铝合金、钢铁均属于金属材料 |
| C.动物油、植物油、矿物油均属于酯类化合物 |
| D.稀豆浆、稀盐酸、硅胶均属于胶体 |
下列过程没有发生化学反应的是
| A.用氢氟酸来刻蚀玻璃器皿 | B.用活性炭去除冰箱中的异味 |
| C.用煤液化和气化得到清洁燃料 | D.用热碱溶液清除炊具上残留的油污 |
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:
X2(g)+3Y2(g)  2XY3(g) ΔH=—92.6KJ/mol
2XY3(g) ΔH=—92.6KJ/mol
实验测得反应在起始、达到平衡时的有关数据如下表所示:
下列叙述不正确的是
| A.容器①、②中反应的平衡常数相等 |
| B.达平衡时,两个容器中XY3的物质的量浓度均为2 mol/L |
| C.容器②中反应达到平衡时放出的热量为Q |
| D.若将容器①体积缩小为0.20 L,则达平衡时放出的热量大于23.15 kJ |
下列根据实验操作和现象所得出的结论,正确的是
| 选项 |
实验操作 |
实验现象 |
结论 |
| A |
向某钠盐溶液中滴加稀硫酸 |
产生能够使石灰水变浑浊的气体 |
该溶液中一定含有CO32-或HCO3- |
| B |
KIO3溶液中加入HI溶液,并加入淀粉 |
溶液变蓝色 |
KIO3的氧化性比I2强 |
| C |
向Na2S溶液中滴加盐酸 |
产生臭鸡蛋气味的气体 |
氯的非金属性比硫强 |
| D |
CO还原Fe2O3得到的黑色固体加入盐酸溶解后,再加入KSCN溶液 |
溶液不显红色 |
黑色固体中无Fe3O4 |