下列有关现象及对应的离子方程式或化学反应方程式不正确的是:
| A.酸性高锰酸钾可使草酸溶液褪色,其离子方程式为: 2MnO4-+ 5C2O42- + 16H+ = 2Mn2++ 10CO2 ↑+ 8H2O |
| B.S2O32-在酸性环境中不存在,其反应的离子方程式为: S2O32-+ 2H+ = S↓ + SO2↑ + H2O |
C.K2Cr2O7在水中存在平衡:Cr2O72- + H2O  2 CrO42- + 2H+ 2 CrO42- + 2H+可由溶液颜色判断其酸碱性 |
| D.SOCl2是一种液态化合物,遇水有雾及刺激性气味气体产生,其化学反应方程式为: |
SOCl2 + H2O = 2HCl↑ + SO2↑
下列实验操作正确的是
| A.盛放NaOH溶液时,使用带玻璃塞的磨口瓶 |
| B.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
| C.NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热 |
| D.做“钠与水的反应”实验时,切取绿豆大小的金属钠,用滤纸吸干其表面的煤油,放入烧杯中,滴入两滴酚酞溶液,再加入少量水,然后观察并记录实验现象 |
设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.1 molCH4分子中共价键总数为NA |
| B.水的摩尔质量就是NA个水分子的质量之和 |
| C.含NA个Na+的Na2O2溶于1L水中,Na+的物质的量浓度为1mol/L |
| D.1 mol Mg与足量O2或N2反应生成MgO或Mg3N2均失去2NA个电子 |
工业上可用软锰矿(主要成分为MnO2)和闪锌矿(主要成分为ZnS)制取干电池中所需的MnO2和Zn,其工艺流程如下: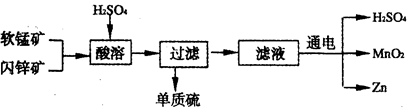
下列说法正确的是
| A.酸溶时,MnO2作还原剂 | B.可用盐酸代替硫酸进行酸溶 |
| C.原料硫酸可以循环使用 | D.在电解池的阴极处产生MnO2 |
下列关于有机物的说法中,不正确的是
| A.2-甲基丁烷和正戊烷互为同分异构体 |
| B.氯乙烯分子内所有原子均在同一平面 |
| C.乙醇可以被氧化为乙酸,二者都能发生酯化反应 |
| D.苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 |
2013年元月,包括开封在内的多个地区发生持续雾霾天气,“PM2.5”数据监测纳入公众视野。PM2.5是指大气中直径小于或等于2.5微米(1微米=10-6米)的可入肺的有害颗粒。下列有关说法中不正确的是
| A.PM2.5在空气中形成了气溶胶 |
| B.PM2.5表面积大能吸附大量的有毒、有害物质 |
| C.研制开发燃料电池汽车,降低机动车尾气污染,某种程度可以减少PM2.5污染 |
| D.PM2.5主要来自工业生产、汽车尾气排放等过程中经过燃烧而排放的残留物,大多含有重金属等有毒物质 |