常温下,下列溶液的pH或微粒的物质的量浓度关系正确的是( )
A.某物质的溶液中由水电离出的c(H+)=1×10-a mol/L,若a>7时,则该溶液的pH一定为14-a
B.某溶液中存在的离子有S2-、HS-、OH-、Na+、H+,则离子浓度一定是
c(Na+) >c(S2-) >c(OH-) >c(HS-) >c(H+)
C.pH=3的二元弱酸H2R溶液与 pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:c(R2-)+ c(HR-)=c(Na+)
D.将0.2 mol/L的某一元酸HA溶液和0.1mol/L NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:2c(OH-)=2c(H+)+c(HA)-c(A-)
已知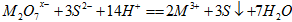 中的M的化合价为
中的M的化合价为
| A.+2 | B.+3 | C.+4 | D.+6 |
将一定量的CO2通入下列溶液中,一定变浑浊的是
| A.CaCl2溶液 | B.澄清石灰水 |
| C.饱和Na2CO3溶液 | D.稀H2SO4 |
下列反应中,水既不是氧化剂又不是还原剂的氧化还原反应是
| A.Na2O和H2O | B.Na和H2O |
| C.电解水 | D.Na2O2和H2O |
下列物质既能与烧碱溶液反应,又能与盐酸溶液反应的是
| A.Na2O | B.Na2CO3 | C.NaOH | D.NaHCO3 |
下列有关Na2CO3和NaHCO3性质的比较中,正确的是
| A.固体的热稳定性:Na2 CO3>NaHCO3 |
| B.与稀盐酸反应放出气体的快慢:Na2CO3>NaHCO3 |
| C.106gNa2CO3和84gNaHCO3分别与过量的盐酸反应,放出CO2的质量:Na2CO3>NaHCO3 |
| D.在Na2CO3和NaHCO3的稀溶液中,加CaCl2溶液都有白色沉淀生成。 |