向一容积为1L 的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)  bZ(g);△H<0。右图是容器中X、Z的物质的量浓度随时间变化的曲线。下列说法正确的是( )
bZ(g);△H<0。右图是容器中X、Z的物质的量浓度随时间变化的曲线。下列说法正确的是( )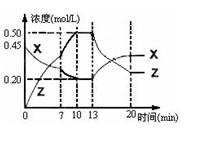
| A.用X表示0~10min内该反应的平均速率为0.025 mol/(L·min) |
| B.根据上图可求得方程式中a:b=2:1 |
| C.0~10min 容器内气体的压强逐渐增小 |
| D.第13min时曲线变化的原因可能是增加了Z的量 |
某有机物A是农药生产中的一种中间体,其结构简式为O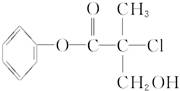 ,下列叙述正确的是 ( )
,下列叙述正确的是 ( )
| A.有机物A属于芳香烃 |
| B.有机物A可以和Br2的CCl4溶液发生加成反应 |
| C.有机物A和浓硫酸混合加热,可以发生消去反应 |
| D.1 mol A和足量的NaOH溶液反应,最多可以消耗3 mol NaOH |
二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命。其结构式为HO—CH2—CH2—O—CH2CH2—OH。下列有关二甘醇说法正确的是( )
| A.不能发生消去反应 |
| B.能发生取代反应 |
| C.能溶于水,不溶于乙醇 |
| D.符合通式CnH2nO3 |
美国媒体2006年3月15日报道:某牙膏中含有的消毒剂三氯生,遇含氯的自来水能生成氯仿,氯仿能导致肝病甚至癌症,已知三氯生的结构简式为: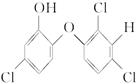 ,下列有关说法不正确的是( )
,下列有关说法不正确的是( )
| A.三氯生的分子式为C12H7Cl3O2 |
| B.氯仿不存在同分异构体 |
| C.三氯生能与NaOH溶液反应 |
| D.三氯生易溶于水 |
我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂。某种兴奋剂的结构简式为下图,有关该物质的说法不正确的是( )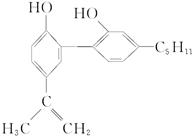
| A.遇FeCl3溶液显紫色,因为该物质与苯酚可视为同一类物质 |
| B.滴入KMnO4酸性溶液,观察到紫色褪去,可证明结构中存在碳碳双键 |
| C.1 mol该物质与浓溴水和H2反应时最多消耗Br2和H2分别为4 mol、7 mol |
| D.该分子中的所有原子不可能共平面 |
某有机物的结构简式为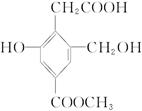 ,现将Na、NaOH、NaHCO3分别与等物质的量的该有机物恰好反应时,消耗Na、NaOH、NaHCO3的物质的量之比为( )
,现将Na、NaOH、NaHCO3分别与等物质的量的该有机物恰好反应时,消耗Na、NaOH、NaHCO3的物质的量之比为( )
| A.3∶3∶2 | B.3∶3∶1 | C.3∶2∶1 | D.3∶2∶2 |