把SO2通入Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀。在上述一系列变化过程中,最终被还原的是
| A.SO2 | B.Cl- | C.Fe3+ | D.NO3- |
某溶液中存在较多的OH—、K+、CO32—,该溶液中还可能大量存在的是
| A.SO42— | B.Ca2+ | C.NH4+ | D.H+ |
在2 L溶有0.2mol NaCl和0.2mol MgCl2的溶液中,Cl—的物质的量浓度为
| A.0.05 mol/L | B.0.1 mol/L | C.0.2 mol/L | D.0.3 mol/L |
含6.02×1023个原子的氧气在标准状况下所占的体积是
| A.44.8 L | B.22.4 L | C.11.2 L | D.5.6 L |
某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;② CO和CO2都是酸性氧化物;③蔗糖、硫酸钡分别属于非电解质和电解质;④CuO和Fe2O3都是碱性氧化物;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦NaCl和KCl可用焰色反应鉴别。上述说法正确的是
| A.①②③④ | B.①③④⑦ | C.③⑤⑥⑦ | D.①②⑤⑥ |
下列离子方程式书写正确的是
| A.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl- |
| B.AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓ |
C.三氯化铁溶液中加入铜粉: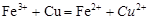 |
| D.铝粉投入到NaOH溶液中:2Al+2OH-══ 2AlO2-+H2↑ |