在酸性溶液中能大量共存,并且溶液为无色透明的离子组是 ( )
| A.NH+4、SO42—、Al3+、Cl— | B.K+、NO3—、Na+、AlO—2 |
| C.Mg2+、SO42—、CO32—、K+ | D.K+、SO42—、MnO4—、NH4+ |
下图所示为某晶体的一个晶胞,该晶体由A、B、C三种基本粒子组成。试根据晶胞判断,该晶体的化学式为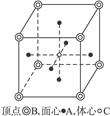
A.A6B8C B.A2B4C C.A3BC D.A3B4C
下列叙述肯定正确的是
| A.在离子晶体中不可能存在非极性键 |
| B.在共价化合物的分子晶体中不可能存在离子键 |
| C.全由非金属元素组成的化合物一定是共价化合物 |
| D.直接由原子构成的晶体一定是原子晶体 |
能用键能大小解释的是
| A.N2的化学性质比O2稳定 |
| B.常温常压下,溴呈液态,碘呈固态 |
| C.稀有气体一般很难发生化学反应 |
| D.硝酸易挥发而磷酸难挥发 |
氮化铝(AlN)是一种熔点很高、硬度大、不导电、难溶于水和其他溶剂的晶体。将下列各组物质加热熔化或汽化,所克服粒子间的作用力与AlN克服粒子间的作用力都相同的是
| A.水晶,金刚石 |
| B.食盐,硫酸钾 |
| C.碘,硫 |
| D.石墨,硅 |
X是核外电子数最少的元素,Y是地壳中含量最丰富的元素,Z在地壳中的含量仅次于Y,W可以形成自然界中最硬的原子晶体。下列叙述错误的是
| A.WX4是沼气的主要成分 |
| B.固态X2Y是分子晶体 |
| C.ZW是原子晶体 |
| D.ZY2的水溶液俗称“水玻璃” |