现有mg某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。
若阿伏加德罗常数用NA表示
(1)该气体的物质的量为________mol。
(2)该气体所含原子总数为_______ _个。
(3)该气体在标准状况下的体积为____________L。
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为______ _。
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为_____ 。
有0.2 mol某有机物和0.5 mol氢气在一密闭容器中燃烧所得产物为二氧化碳、一氧化碳和水蒸气。产物依次通过浓H2SO4时,浓H2SO4的质量增加了10.8 g;再通过灼热的氧化铜时,氧化铜的重量减轻了3.2 g;又通过碱石灰时,碱石灰的质量增加了17.6 g,求有机物的分子式,并写出其可能的结构简式。
在化工分析中常用到滴定度这个概念。滴定度是指每毫升滴定剂标准溶液相当于被测组分的质量,其单位为g·mL-1。现有一不溶于水的氧化亚铜样品,该样品能溶于用硫酸酸化了的硫酸铁溶液,所发生反应的化学方程式为(未配平):
Cu2O+Fe2(SO4)3+H2SO4 CuSO4+FeSO4+H2O。反应生成的硫酸亚铁用硫酸酸化了的高锰酸钾溶液进行滴定,其滴定反应的化学方程式为(未配平):
CuSO4+FeSO4+H2O。反应生成的硫酸亚铁用硫酸酸化了的高锰酸钾溶液进行滴定,其滴定反应的化学方程式为(未配平):
KMnO4+H2SO4+FeSO4 Fe2(SO4)3+MnSO4+K2SO4+H2O
Fe2(SO4)3+MnSO4+K2SO4+H2O
若每升滴定剂溶液中含有0.400 mol KMnO4,求该KMnO4溶液对Cu2O的滴定度。
难溶化合物的饱和溶液存在溶解平衡,例如:AgCl(s) Ag++Cl-,Ag2CrO4(s)
Ag++Cl-,Ag2CrO4(s) 2Ag++
2Ag++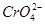 ,在一定温度下,其离子浓度乘积为常数,这一常数叫溶度积常数,用Ksp表示,已知:Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=[c(Ag+)]2·c(
,在一定温度下,其离子浓度乘积为常数,这一常数叫溶度积常数,用Ksp表示,已知:Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=[c(Ag+)]2·c(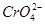 )=1.9×10-12,现用0.01 mol·L-1 AgNO3溶液滴定0.01 mol·L-1 KCl和0.001 mol·L-1 K2CrO4混合溶液,通过计算完成下列问题:
)=1.9×10-12,现用0.01 mol·L-1 AgNO3溶液滴定0.01 mol·L-1 KCl和0.001 mol·L-1 K2CrO4混合溶液,通过计算完成下列问题:
(1)Cl-、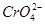 谁先沉淀?
谁先沉淀?
(2)当刚出现Ag2CrO4沉淀时,溶液中Cl-浓度是多少?(设混合溶液在反应中体积不变)
铬酸银在298 K时的溶解度为0.004 45 g,求其溶度积。
取1.43g Na2CO3·xH2O 溶于水配成10mL溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸 2.0m L,并收集到112m LCO2(标准状况)。
求(1)稀盐酸物质的量浓度(2)Na2CO3·XH2O 的摩尔质量(3)x值