在2L的密闭容器中,发生3A(g)+B(g) 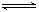 2C(g)的反应,若最初加入A和B都是4mol,10s后,测得υ(A)=0.12mol/(L•s),则此时容器中B的物质的量是
2C(g)的反应,若最初加入A和B都是4mol,10s后,测得υ(A)=0.12mol/(L•s),则此时容器中B的物质的量是
A.2.4mol B.0.8mol C.3.2mol D.1.6mol
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是
A.反应的化学方程式:2N M M |
| B.t2时,正、逆反应速率相等,达到平衡 |
| C.t3时,正反应速率大于逆反应速率 |
| D.反应开始时只投入了N |
某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g) Z(g)+W(s) ΔH>0下列叙述正确的是
Z(g)+W(s) ΔH>0下列叙述正确的是
| A.加入少量W,逆反应速率增大 |
| B.升高温度,平衡逆向移动 |
| C.当容器中气体压强不变时,反应达到平衡 |
| D.平衡后加入X,上述反应的ΔH增大 |
下列叙述正确的是
| A.常温下,反应C(s) + CO2(g)=2CO(g)不能自发进行,则该反应△H>0 |
| B.强电解溶液的导电能力一定强于弱电解质溶液的导电能力 |
| C.CH3COOH、Cu(OH)2、BaSO4、NH3都是常见的弱电解质 |
| D.常温下就能发生的化学反应一定是放热反应 |
下列溶液一定呈中性的是
A.溶液中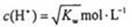 (KW为溶液所处温度时水的离子积常数) (KW为溶液所处温度时水的离子积常数) |
| B.pH=7的溶液 |
| C.使石蕊试液呈紫色的溶液 |
| D.等体积0.1 mol·L-1硫酸与0.1 mol·L-1的氢氧化钠溶液混合后的溶液 |
已知热化学方程:

为提供分解1molKNO3所需的能量,理论上需完全燃烧碳
| A.58/94mol | B.58/(94×2) mol | C.(58×2)/94mol | D.(94×2)/58mol |