下列各组物质的颜色变化,可用勒夏特列原理解释的是
| A.新制的氯水在光照条件下颜色变浅 |
| B.H2、I2、HI平衡混合气加压后颜色变深 |
| C.KI溶液加氯水振荡后颜色变深 |
| D.加入催化剂有利于氨氧化的反应 |
X元素的阳离子和Y元素的阴离子具有相同的电子层结构,下列叙述正确的是
| A.原子序数X<Y | B.离子半径X<Y |
| C.原子半径X<Y | D.原子最外层电子数X>Y |
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等。下列判断不正确的是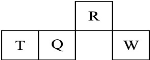
| A.最高价氧化物对应水化物的酸性:Q<W |
| B.最简单气态氢化物的热稳定性:R>Q |
| C.含T的盐中,T元素只能存在于阳离子中 |
| D.原子半径:T>Q>R |
下列物质中,含有非极性共价键的是
| A.CO2 | B.NaOH | C.CH4 | D.Na2O2 |
下列关于元素周期表和元素周期律的说法错误的是
| A.因为Na比K容易失去电子,所以Na比K的还原性强 |
| B.N与P为同主族元素,且N比P的非金属性强 |
| C.Li、Na、K原子的电子层数随着核电荷数的增加而增多 |
| D.第3周期元素从Na到Cl,非金属性逐渐增强 |
将14g铜银合金跟足量的某浓度HNO3反应,将放出的气体与1.12LO2(标准状况)混合,通入水中,恰好全部吸收,则合金中银的质量是
| A.3.2g | B.10.8g | C.21.6g | D.5.4g |