已知某KOH样品中含水7.62%,含K2CO32.23%,含KOH90%。现将1.00g样品加入46.00mL1.00mol/L的盐酸中,过量的酸用1.070mol/LKOH溶液刚好中和。蒸发溶液,蒸发到无水时,可得到固体的质量约为
| A.3.00g | B.3.43g | C.4.50g | D.无法计算 |
在2A(g)+B(g) 3C(g)+4D(g)反应中,表示该反应速率最快的是
3C(g)+4D(g)反应中,表示该反应速率最快的是
| A.vA=0.05mol/(L·s) | B.vB=0.03mol/(L·s) |
| C.vC=3.6mol/(L·min) | D.vD=0.1mol/(L·s) |
下列有关右图表示的反应叙述正确的是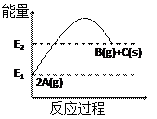
A.1molC(s)的能量高于2molA(g)能量
B.该反应的热化学方程式为:2A(g)=" B(g)+C(s)" △H=(E1-E2)kJ/mol
C.反应过程中当v(A)=0.4mol/(L·s),则v(C)=0.2mol/(L·s)
D.该反应为吸热反应
下列有关能源叙述不正确的是
| A.沼气是不可再生能源 | B.太阳能是新能源 |
| C.石油是化石燃料 | D.风能是一次能源 |
某无色溶液,由Na+、Ba2+、Al3+、AlO2-、Fe3+、CO32-、SO42-中的若干种组成。取适量该溶液进行如下实验:①加入过量盐酸,有气体生成;②在①所得的溶液中再加入过量碳酸氢铵溶液,有气体生成,同时析出白色沉定甲;③在②所得溶液中加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出。原溶液中一定存在的离子是
| A.Al3+、Fe3+、SO42- | B.Na+、AlO2-、CO32- |
| C.Na+、AlO2-、SO42-、CO32- | D.Na+、Ba2+、AlO2- |
将足量稀盐酸加到下列固体混合物中,只能发生一种反应的是()
| A.Mg、AlCl3、NaAlO2 | B.KNO3、NaCl、CH3COONa |
| C.NaClO、 Na2SO3、BaCl2 | D.Ba(NO3)2、 FeSO4、NH4HCO3 |