除去下列物质中的杂质(括号内为杂质),所选用的试剂及操作方法均正确的一组是
| 选项 |
待提纯的物质 |
选用的试剂 |
操作的方法 |
| A |
CaO(CaCO3) |
水 |
溶解、过滤、结晶 |
| B |
Cu(CuO) |
稀盐酸 |
溶解、过滤、洗涤、干燥 |
| C |
CuSO4(H2SO4) |
氢氧化钠溶液 |
过滤 |
| D |
CO(H2) |
氧气 |
点燃 |
下列反应的离子方程式表示正确的是()
| A.H2O2溶液与酸性KMnO4溶液反应:2MnO4-+3H2O2+6H+=2Mn2++6H2O+4O2↑ |
| B.向Fe(NO3)3溶液中加入过量的HI溶液:2 NO3-+8H++6I-=3I2+2NO↑+4H2O |
| C.少量SO2通入碳酸钠溶液中:CO32-+SO2=CO2+SO32- |
| D.0.01 mol·L-1 NH4Al(SO4)2溶液与0.02 mol·L-1 Ba(OH)2溶液等体积混合: |
NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O
下列离子或分子在溶液中能大量共存,通入CO2后仍能大量共存的一组是
| A.K+、Ca2+、F-、NO | B.K+、Ba2+、Br-、NO |
| C.Na+、K+、CO32-、HCO3- | D.Na+、Ag+、NH3·H2O、NO |
下列各项内容中,排列顺序正确的是()
①固体的热稳定性:Na2CO3>CaCO3>NaHCO3 ②物质的熔点Li>Na>K③微粒半径:K+>S2->F- ④单质的密度Na<K<Rb ⑤氢化物的沸点:H2Se>H2S>H2O
| A.①③⑤ | B.①②④ | C.④⑤ | D.①② |
根据原子结构及元素周期律的知识,下列推断正确的是()
| A.同周期元素含氧酸的酸性随核电荷数的增加而增强 |
| B.核外电子排布相同的微粒化学性质也相同 |
| C.Cl‾、S2‾、K+、Ca2+半径逐渐减小 |
D.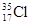 与 与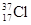 得电子能力相同 得电子能力相同 |
下列说法正确的是()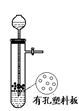


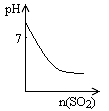
图Ⅰ图Ⅱ图Ⅲ图Ⅳ
| A.图I所示装置用于Cu和浓H2SO4制取少量的SO2气体 |
| B.图Ⅱ装置可验证非金属性:Cl>C>Si |
| C.图Ⅲ可用于收集气体H2、CO2、Cl2、NH3 |
| D.图Ⅳ表示将SO2气体通入溴水中,所得溶液的pH变化 |