已知:断裂下列化学键需要吸收的能量分别为:
H-H 436 kJ/mol;F—F 153 kJ/mol;H—F 565 kJ/mol。
下列说法正确的是 ( )
| A.H2与F2反应的热化学方程式为:H2(g) + F2(g) = 2HF(g)△H =" -541" kJ |
| B.2 L HF气体分解成1 L H2和1 L F2吸收541 kJ的热量 |
| C.1 mol H2与1 mol F2反应生成2 mol液态HF放出热量小于541 kJ |
| D.在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量 |
700℃时,向容枳为2L的密闭容器中充入一定量的CO和H2O发生反应:
CO(g)+H2O(g) 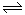 CO2+H2(g)
CO2+H2(g)
反应过程中测定的部分数据见表。下列说法正确的是
| A.反应在t1min内的平均速率为v (H2)=0.4/t1 mol·L-1·min-1 |
| B.其他条件不变,起始时向容器中充入0.60molCO和1.20 mo1H2O,到达平衡时,n(CO2)="0.40" mol |
| C.其他条件不变,向平衡体系中再通入0.2molH2O,达到新平衡时CO转化率减小 |
| D.温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应 |
下列表格中的图示内容符合要求的是
下列说法中,不正确的是
| A.向空气中大量排放SO2和NO2都能引起酸雨和光化学烟雾 |
| B.不法分子制作假鸡蛋用的海藻酸钠、氯化钙以及碳酸钙都属于盐 |
| C.明矾用于净水既与盐类的水解有关,又与胶体的性质有关 |
| D.FeS难溶于水(KSP=6.3×10-18),但能除去水中的Cu2+(CuS的KSP =1.3×10-36) |
某溶液中含有的溶质是FeBr2、FeI2,若先向该溶液中通入一定是的氯气。再向反应后的溶液中滴加KSCN溶液,溶液变为红色,则下列叙述正确的是
①原溶液中的Br-一定被氧化;
②通入氯气之后原溶液中的Fe2+一定有部分或全部被氧化;
③不能确定通入氯气后的落液中是否存在Fe2+
④若取少量所得溶液,再加入CCl4溶液充分振荡,静置、分液,向上层溶液中加入足量的AgNO3溶液,只产生白色沉淀,说明原溶液中的I-、Fe2+、Br-均被完全氧化
A.①②③B.②③④C.①③④D①②③④
下列叙述中正确的是
| A.液溴应保存于带磨口玻漓塞的广口试剂瓶中,并加水“水封”以减少其易挥发 |
| B.向Ca(ClO)2溶液通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 |
| C.滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸不变蓝,原溶液中无NH4+ |
| D.氨气是一种碱性气体,可用P2O5或无水CaCl2干燥 |