常温下,某强酸溶液的PH=a,强碱溶液的PH=b,已知a+b=12,酸碱溶液混合后PH=7,则酸溶液的体积V(酸)和碱溶液体积V(碱)的正确关系是:A
| A.V(酸)=102V(碱) | B.V(碱)=102V(酸) |
| C.V(酸)=2V(碱) | D.V(碱)=2V(酸) |
在含有1 mol FeSO4的溶液中投入一小块金属钠,反应完全后,滤出沉淀并洗涤,然后在空气中灼烧沉淀,得到的固体物质是( )
| A.Fe | B.FeO | C.Fe(OH)3 | D.Fe2O3 |
在稀硫酸中加入铜粉,铜粉不溶,再加入下列物质:①FeCl3②Fe2O3③Cu(NO3)2④KNO3,铜粉溶解的是( )
| A.只有①或② | B.只有②或④ |
| C.只有①或②或③ | D.上述四种物质中任意一种 |
某同学研究铝及其化合物的性质时设计了如下两个实验方案。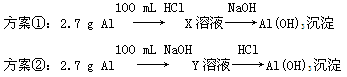
NaOH和HCl的浓度均是3 mol/L,如图是向X溶液和Y溶液中分别加入NaOH和HCl时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法不正确的是( )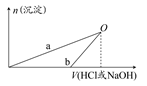
| A.b曲线表示的是向X溶液中加入NaOH溶液 |
| B.在O点时两方案中所得溶液浓度相等 |
| C.a、b曲线表示的反应都是非氧化还原反应 |
| D.X溶液显酸性,Y溶液呈碱性 |
双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式是NaAl(OH)2CO3。关于该物质的说法正确的是( )
| A.该物质属于两性氢氧化物 |
| B.该物质是Al(OH)3和Na2CO3的混合物 |
| C.1 mol NaAl(OH)2CO3最多可消耗3 mol H+ |
| D.该药剂不适合于胃溃疡患者服用 |
某溶液中可能含有大量的Mg2+、Al3+、H+、Cl-和少量OH-,向该溶液中逐滴加入0.5 mol·L-1的NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如图所示,则该溶液中( )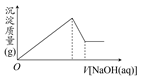
| A.有Mg2+,没有Al3+ |
| B.有Al3+,没有Mg2+ |
| C.有大量的H+、Mg2+和Al3+ |
| D.有Mg2+和Al3+ |