设NA为阿伏伽德罗常数,下列叙述正确的是
| A.24g镁原子最外层电子数为NA | |
B.1L0.1mol·L-1乙酸溶液中H+数为0.1NA |
C.1mol甲烷分子所含质子数为10NA |
| D.标准状况下,22.4L乙醇的分子数为NA |
下列各表述与示意图一致的是
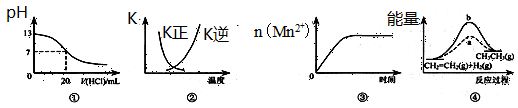
| A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
B.图②中曲线表示反应2SO2(g) + O2(g) 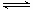 2SO3(g);ΔH<0 正、逆反应的平衡常数K随温度的变化 2SO3(g);ΔH<0 正、逆反应的平衡常数K随温度的变化 |
| C.图③表示10 mL 0.01 mol·L-1 KMnO4酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化 |
| D.图④中a、b曲线分别表示反应CH2=CH2 (g) + H2(g)→CH3CH3(g);ΔH<0使用和未使用催化剂时,反应过程中的能量变化 |
在四个不同的容器中进行合成氨的反应。根据下列在相同时间内测定的结果,判断生成氨的速率最快的是
| A.v (N2)=0.05mol·L-1·s-1 | B.v (H2)=0.3mol·L-1·min-1 |
| C.v (N2)=0.2 mol·L-1·min-1 | D.v (NH3)=0.3 mol·L-1·min-1 |
运用有关概念判断下列叙述正确的是
| A.1molH2燃烧放出的热量为H2的燃烧热 |
| B.Na2SO3与H2O2的反应为氧化还原反应 |
C.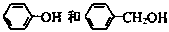 互为同系物 互为同系物 |
| D.BaSO4的水溶液不易导电,故BaSO4是弱电解质 |
如下图所示,△H1=-393.5 kJ•mol-1,△H2=-395.4 kJ•mol-1,下列说法或表示式正确的是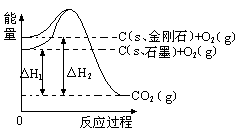
| A.石墨和金刚石的转化是物理变化 |
| B.1mol石墨的总能量比1 mol金刚石的总能量大1.9 kJ |
| C.金刚石的稳定性强于石墨 |
| D.C(s、石墨)=C(s、金刚石) △H=" +1.9" kJ•mol-1 |
在同温同压下,下列各组热化学方程式中,△H2>△H1的是
| A.S(g)+O2(g)=SO2(g),△H1; S(s)+O2(g)=SO2(g),△H2 |
| B.2H2(g)+O2(g)=2H2O(g),△H1; 2H2(g)+O2(g)=2H2O(l),△H2 |
C.C(s)+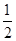 O2(g)=CO(g)△H1;C(s)+O2(g)=CO2(g) △H2 O2(g)=CO(g)△H1;C(s)+O2(g)=CO2(g) △H2 |
| D.H2(g)+Cl2(g)=2HCl(g),△H1; 2H2(g)+2Cl2(g)=4HCl(g),△H2 |