将一定量的Fe、 、CuO的混合物放入体积为100mL、浓度为2.2mol·L-1的
、CuO的混合物放入体积为100mL、浓度为2.2mol·L-1的 溶液中,充分反应后,生成气体896mL(标况),得到不溶固体1.28g,过滤后,滤液中的金属离子只有
溶液中,充分反应后,生成气体896mL(标况),得到不溶固体1.28g,过滤后,滤液中的金属离子只有 (滤液体积仍为100mL)。向滤液滴加
(滤液体积仍为100mL)。向滤液滴加 2mol·L-1的NaOH溶液至40mL时开始出现沉淀。则未滴加NaOH溶液前滤液中FeSO4的物质的量浓度为
2mol·L-1的NaOH溶液至40mL时开始出现沉淀。则未滴加NaOH溶液前滤液中FeSO4的物质的量浓度为
| A.2mol·L-1 | B.1.8mol·L- | C.1.9mol·L-1 | D.无法计算 |
下列实验操作均要用玻璃棒,其中玻璃棒的作用及其目的相同的是
①过滤②蒸发③溶解④向容量瓶转移液体
| A.①和② | B.①和③ | C.③和④ | D.①和④ |
有A、B、C、D四种金属,将A与B用导线连接起来浸入电解质溶液中,A被腐蚀;将A、D分别投入等浓度的盐酸中,D比A反应剧烈;将铜浸入B的盐溶液中,无明显变化;若将铜浸入C的盐溶液中,有金属C析出。据此判断这四种金属的活动性由强到弱的顺序是
A.D>C>A>B B.D>A>B>C C.D>B>A>C D.B>A>D>C
A、B、C三支试管中分别盛有Cl-、Br-、I-的溶液,向A试管中加入新制的氯水和CCl4,出现分层,下层为橙红色,再将此溶液倒入C试管中,无变化,则A、B、C三支试管中所盛有的离子依次是
A.I-、Br-、Cl- B.Br-、I-、Cl-C.Cl-、I-、Br- D.Br-、Cl-、I-
A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是
A.A、B、C、D、E B.E、C、D、B、A
C.B、A、D、C、E D.C、D、A、B、E
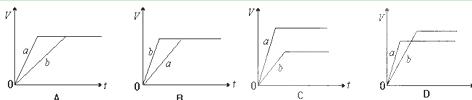
等质量的两份锌粉a、b,分别加入过量的稀H2SO4,同时向a中加入少量的CuSO4溶液,下列图表示产生H2的体积(V)与时间(t)的关系,其中正确的是