将一定量的 通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中
通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中 和
和 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法正确的是
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法正确的是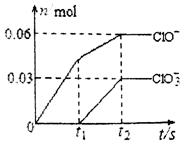
| A.苛性钾溶液中KOH的质量是4.94g |
| B.反应中转移电子的物质的量是0.21mol |
C. 的物质的量为0.09mol 的物质的量为0.09mol |
D. 的生成是由于KOH过量引起的 的生成是由于KOH过量引起的 |
目前,我国城市环境污染中的大气污染物主要是
| A.NH3、NO、CO2、雾 |
| B.CO2、N2、Cl2、酸雨 |
| C.SO2、NO2、CO、烟尘 |
D.HC l、SO2、N2、沙尘暴 l、SO2、N2、沙尘暴 |
下列各组混合物,不能用分液漏斗分开的是①四氯化碳、水②乙醇、甘油③乙醇、水 ④苯、水⑤已烷、水⑥环已烷、苯⑦溴苯、水
④苯、水⑤已烷、水⑥环已烷、苯⑦溴苯、水
| A.①②③ | B.②③⑥ | C.①④ ⑤⑦ ⑤⑦ |
D.④⑤⑥ |
下列物质属于醇类的是
A. |
B.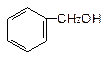 |
C. |
D.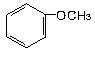 |
下列有机反应中,不属于取代反应的是
A. +Cl2 +Cl2 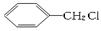 +HCl +HCl |
B.2CH3CH2OH+O2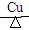 2CH3CHO+2H2O 2CH3CHO+2H2O |
C.ClCH2CH===CH2+ NaOH HOCH2CH===CH2+NaCl HOCH2CH===CH2+NaCl |
D. +HO—NO2 +HO—NO2  +H2O +H2O |
乙醇分子中各种化学键如下图所示,关于乙醇在各种反应中断裂键的说法不正确的是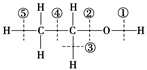
| A.和金属钠反应时键①断裂 |
| B.和浓H2SO4共热到170℃时键②和⑤断裂 |
| C.和浓H2SO4共热到140℃时仅有键②断裂 |
| D.在Ag催化下与O2反应时键①和③断裂 |