下列物质的名称及其所对应的化学式均正确的是
| A.乙酸乙脂:CH3COOCH2CH3 | B.羟基:HO— |
| C.小苏打:Na2CO3 | D.氨根离子:NH4+ |
在恒容密闭容器中,可以作为2NO2(g) 2NO(g)+O2(g)达到平衡状态的标志是:①单位时间内生成n mol O2的同时生成2n mol NO2;②单位时间内生成n mol O2的同时生成2n mol NO;③混合气体的颜色不再改变;④混合气体的密度不再改变的状态;⑤混合气体的平均相对分子质量不再改变的状态;⑥混合气体中NO与O2的物质的量之比保持恒定;⑦混合气体中NO与NO2的物质的量之比保持恒定
2NO(g)+O2(g)达到平衡状态的标志是:①单位时间内生成n mol O2的同时生成2n mol NO2;②单位时间内生成n mol O2的同时生成2n mol NO;③混合气体的颜色不再改变;④混合气体的密度不再改变的状态;⑤混合气体的平均相对分子质量不再改变的状态;⑥混合气体中NO与O2的物质的量之比保持恒定;⑦混合气体中NO与NO2的物质的量之比保持恒定
| A.①③⑤⑦ | B.②④⑤ | C.①③④ | D.①②③④⑤ |
表面介导电池(SMCS)是一种新型充电电池,可使电动汽车的充电时间仅需几分钟,该电池的电极材料为金属锂和氧化石墨烯。下列有关说法中不正确的是
| A.放电时,氧化石墨烯作正极 |
| B.放电时,负极电极反应式为Li-e-===Li+ |
| C.充电时,该电池是将电能转化为化学能 |
| D.充电时,电解质溶液中的Li+从阴极迁移到阳极 |
已知HCl为强酸,下列对比实验不能用于证明CH3COOH为弱酸的是
| A.对比等浓度的两种酸溶液的pH |
| B.对比等浓度的两种酸溶液,与相同大小镁条反应的初始速率 |
| C.对比等浓度、等体积的两种酸溶液,与等量NaOH溶液反应后放出的热量 |
| D.对比等浓度、等体积的两种酸溶液,与足量Zn反应,生成H2的体积 |
常温下,下列各组离子在指定溶液中能大量共存的是
| A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ |
| B.由水电离的c(H+)=1×10-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C.c(H+) / c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- |
| D.c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- |
如图装置中,小试管内为红墨水,带有支管的U型管中盛有pH=4的雨水和生铁片。经观察,装置中有如下现象:开始时插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,略高于U型管中的液面。以下有关解释合理的是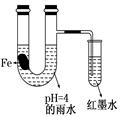
| A.生铁片中的碳是原电池的负极,发生还原反应 |
| B.雨水酸性较强,生铁片始终发生析氢腐蚀 |
| C.墨水液面回升时,正极反应式为:O2+2H2O+4e—==4OH- |
| D.U型管中溶液pH逐渐减小 |