高温下,某反应达平衡,平衡常数 恒容时,温度升高H2浓度减小。下列说法正确的是 ( )
恒容时,温度升高H2浓度减小。下列说法正确的是 ( )
| A.该反应化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g) |
B.恒温恒容下,增大压强 ,H2浓度一定减小 ,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
| D.该反应的焓变为正值 |
下列实验装置(固定装置略去)和操作正确的是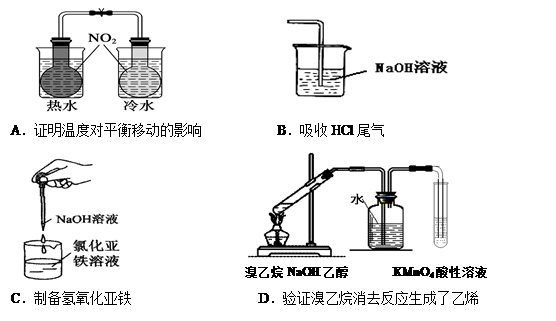
下列陈述Ⅰ、Ⅱ都正确并且有因果关系的是
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
浓硫酸有强氧化性 |
浓硫酸不能用于干燥H2S和HI气体 |
| B |
NH4Cl为强酸弱碱盐 |
用加热法除去NaCl中的NH4Cl |
| C |
溶解度:CaCO3<Ca(HCO3)2 |
溶解度:Na2CO3<NaHCO3 |
| D |
SiO2是两性氧化物 |
SiO2能与NaOH溶液和氢氟酸反应 |
某同学通过系列实验探究Mg及其化合物的性质,操作正确且能达到目的的是
| A.将水加入浓硫酸中得到稀硫酸,置镁条于其中探究Mg的活泼性 |
| B.将NaOH溶液缓慢滴入MgSO4溶液中,观察Mg(OH)2沉淀的生成 |
| C.将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 |
| D.将Mg(OH)2沉淀转入蒸发皿中,加足量稀盐酸,加热蒸干得无水MgCl2固体 |
能在溶液中大量共存的一组离子是
| A.NH4+、Ca2+、SO42-、CO32- | B.Fe3+、H+、I-、HCO3- |
| C.K+、Na+、H+、NO3-、MnO4- | D.Al3+、Mg2+、SO42-、CO32- |
短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是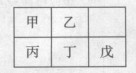
| A.原子半径:丙<丁<戊 |
| B.元素金属性:甲>丙 |
| C.氢氧化物碱性:丙<丁<戊 |
| D.丙的最高价氧化物水化物与戊的最高价氧化物水化物能发生反应 |