下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是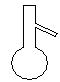

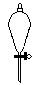

| A.蒸馏、蒸发、萃取、过滤 | B.蒸馏、过滤、萃取、蒸发 |
| C.萃取、过滤、蒸馏、蒸发 | D.过滤、蒸发、萃取、蒸馏 |
250 mL K2SO4和CuSO4的混合溶液中c(SO42-)=0.5 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到1.12 L气体(标准状况下)。假定电解后溶液体积仍为250 mL,下列说法不正确的是
| A.电解得到Cu的质量为3.2 g |
| B.上述电解过程中共转移电子0.2 mol |
| C.电解后的溶液中c(H+)=0.2 mol·L-1 |
| D.原混合溶液中c(K+)=0.6 mol·L-1 |
下列高聚物由两种单体缩聚而成的是
A.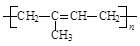 |
B.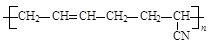 |
C.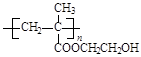 |
D.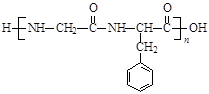 |
下列各组有机物,不论按何种比例混合,只要总质量一定,完全燃烧生成水的总质量就相同的是
| A.甲烷、丙烷 | B.甲苯、甘油 | C.甲酸、乙酸 | D.乙醇、乙二醇 |
对下列各组反应所属类型的判断和书写均正确的是
| A.CaC2与水反应制乙炔,乙烯与水反应制乙醇——水解反应 |
| B.由苯制硝基苯,由甲苯制TNT——消化反应 |
| C.油脂的硬化,油脂的氢化——加聚反应 |
| D.乙醇与酸性K2Cr2O7溶液反应,乙醛与新制Cu(OH)2浊液反应——氧化反应 |
下列实验操作正确且能达到预期目的的是
| 实验目的 |
操作 |
|
| A |
比较水和乙醇中羟基氢的活泼性强弱 |
用金属钠分别与水和乙醇反应 |
| B |
配制银氨溶液 |
向洁净试管中加入1 mL 2%稀氨水,边振荡试管边滴加2%硝酸银溶液至沉淀恰好溶解 |
| C |
欲证明CH2=CHCHO中含有碳碳双键 |
滴入KMnO4酸性溶液,看紫红色是否褪去 |
| D |
检验某病人是否患糖尿病 |
取病人尿液加稀H2SO4,再加入新制Cu(OH)2浊液,加热,看是否有红色沉淀生成 |