下列反应的离子方程式书写正确的是
A.氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++ Cu Cu |
B.稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3+ +3H2↑ +3H2↑ |
| C.氢氧化钡溶液与稀 H2SO4反应:Ba2++SO42-=BaSO4↓ |
D.碳酸钙与盐 酸反应:CO32-+2H+=H2O+CO2↑ 酸反应:CO32-+2H+=H2O+CO2↑ |
下列说法不正确的是
| A.可以用Si3N4、Al2O3制作高温结构陶瓷制品 |
| B.雾霾天气首要污染物为PM2.5(指大气中直径小于或等于2.5微米的颗粒物),PM2.5在空气中一定形成气溶胶 |
| C.化学家鲍林提出了氢键理论和蛋白质分子的螺旋结构模型,为DNA分子双螺旋结构模型的提出奠定了基础 |
| D.据测定,许多反应的温度每升高10K,其反应速率增加2~4倍。在实验室或工业生产中,常采用加热的方法使化学反应在较高的温度下进行,以提高反应速率 |
Na2O2、HCl、Al2O3三种物质在水中完全反应后,溶液中只含有Na+、H+、Cl-、OH-,且溶液呈中性,则Na2O2、HCl、Al2O3的物质的量之比可能为
| A.2︰4︰1 | B.3︰2︰1 | C.2︰3︰1 | D.4︰2︰1 |
下列说法正确的是
| A.工业上利用合成氨实现人工固氮 |
| B.SiO2有导电性,可用于制备光导纤维 |
| C.SO2具有氧化性,可用于漂白纸浆 |
| D.Zn具有还原性和导电性,可用作锌锰干电池的正极材料 |
在T℃时,将ag NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g/cm3,溶质的质量分数为W,其中含NH4+的物质的量为bmol。下列叙述中正确的是
A.溶质的质量分数为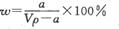 |
B.溶质的物质的量浓度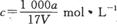 |
C.溶液中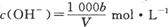 |
| D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于O.5w |
某溶液中含有大量的下列离子:Fe3+、SO42-、Al3+和M离子,经测定Fe3+、SO42-、Al3+和M离子的物质的量之比为2∶4∶1∶1,则M离子可能是下列中的
| A.Na+ | B.Cl- | C.OH- | D.S2- |