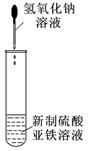
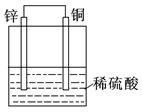
关于下列各装置图的叙述中,正确的是

① ② ③ ④
| A.实验室用装置①制取氨气 |
| B.装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸 |
| C.装置③可用于制备氢氧化亚铁并观察其颜色 |
| D.装置④是原电池,锌电极为负极,发生还原反应 |
在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+===2As+3SnCl+6M,关于该反应的说法中正确的组合是()
①氧化剂 是H3AsO3 ②还原性:Cl->As ③每生成7.5 g As,还原剂失去的电子为0.3 mol ④M为OH- ⑤SnCl是氧化产物
是H3AsO3 ②还原性:Cl->As ③每生成7.5 g As,还原剂失去的电子为0.3 mol ④M为OH- ⑤SnCl是氧化产物
| A.①③⑤ | B.①②④⑤ | C.①②③④ | D.①③ |
在配制一定物质的量浓度的盐酸时,下列错误操作可使所配制溶液的浓度偏高的是
()
| A.用量筒量取浓盐酸时俯视量筒刻度进行读数 |
| B.溶解搅拌时有液体飞溅 |
C.定容时俯视容量瓶瓶颈刻度线 |
| D.摇匀后见液面下降,再加水至刻度线 |
下列各组溶液中,用括号内的试剂及物质间相互反应不能鉴别的一组是()
| A.Ba(OH) 2 KSCN NaCl Mg(NO3)2 (FeCl3溶液) |
| B.NaNO3 NaHCO3(NH4)2SO3 Na2SiO3(H2SO4溶液) |
| C.NH4Br K2CO3 NaI CaCl2(AgNO3溶液) |
| D.(NH4) 3PO4 NaBr CuSO4 AlCl3(KOH溶液) |
过氧化钠具有强碱性和强氧化性,遇木炭、铝粉等还原性物质时可燃烧。下列有关说法中不正确的是()
| A.Na2O2与木炭的反应是放热反应 |
| B.熔融Na2O2时可使用石英器皿 |
| C.Na2O2与Al反应时Na2O2表现出强氧化性 |
| D.Na2O2与SO2反应可生成Na2SO4 |
用10 mL 0.1 mol/L的BaCl2溶液可分别使相同体积的Fe2(SO4)3、ZnSO4和K2SO4三种溶液中的SO完全转化为BaSO4沉淀 ,则三种硫酸盐溶液的物质的量浓度之比是
,则三种硫酸盐溶液的物质的量浓度之比是
()
A.1∶3∶ 3 3 |
B.1 ∶2∶3 ∶2∶3 |
C.3∶2∶2 | D.3∶1∶1 |