下列选项中正确的是
| A.1L0.5mol·L-1稀硫酸与1L1mol·L-1氢氧化钠溶液反应放出57.3kJ的热量: H2SO4(aq) +2Na  OH(aq) = Na2SO4(aq) +2H2O(1);△ H = -57.3 kJ· mol-1 OH(aq) = Na2SO4(aq) +2H2O(1);△ H = -57.3 kJ· mol-1 |
B.某酸的酸式盐NaHY水溶液显碱性,则H2Y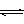 2H++Y2— 2H++Y2— |
C.纯碱溶液显碱性的原因用离子方程式可表示为:CO32—+2H2O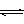 H2CO3+2OH— H2CO3+2OH— |
D.以惰性电极电解KCl溶液的离子方程式为:2Cl-+2H2O  H2↑+2OH-+Cl2↑ H2↑+2OH-+Cl2↑ |
斯坦福大学B.M.Trost教授提出了绿色化学的核心概念——原子经济性。我们常用原子利用率来衡量化学反应过程的原子经济性,其计算公式为:
下面是联合工艺法制备新型自来水消毒剂ClO2,其反应原理由三步组成:
①电解氯化钠溶液NaCl+3H2O NaClO3+3H2↑
NaClO3+3H2↑
②氢气和氯气合成氯化氢
③生成二氧化氯 ↑+
↑+ ↑+
↑+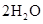
此方法的原子利用率最大为
A.37.6 B.53.6% C.62.2% D.94.4%
X为短周期元素,某溶液中存在 ,则一定能在此溶液中大量共存的离子组是
,则一定能在此溶液中大量共存的离子组是
A.Na+、H+、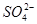 、K+ 、K+ |
B.Na+、Ba2+、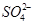 、A13+ 、A13+ |
| C.Na+、K+、Fe2+、H+ | D.K+、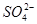 、Cl—、 、Cl—、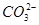 |
已知25℃时,AgC1、AgBr、Agl的Ksp分别为1.8×l0-l0、5.O×10—13、8.3×10—17,用AgNO3标准溶液滴定卤素离子的过程,以滴入AgNO3溶液的体积为横坐标,pX为纵坐标:[pX= -lgc(X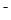 )],就可绘得滴定曲线。现以0.1 mol·L-l AgNO3溶液分别滴定20.00 mL 0.1 mol·L-lCl
)],就可绘得滴定曲线。现以0.1 mol·L-l AgNO3溶液分别滴定20.00 mL 0.1 mol·L-lCl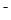 、Br
、Br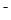 、I
、I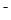 绘得滴定曲线如图,下列有关说法中正确的是
绘得滴定曲线如图,下列有关说法中正确的是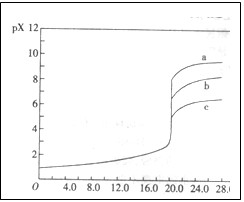
A.a、b、c分别表示Cl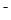 、Br 、Br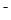 、I 、I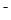 |
B.a、b、c分别表示I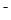 、Br 、Br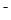 、Cl 、Cl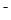 |
C.a、b、c分别表示Br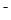 、I 、I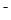 、Cl 、Cl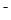 |
D.用硝酸银滴定法测定试样中c(Cl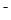 ),可用KI作指示剂 ),可用KI作指示剂 |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
下列叙述错误的是:
| A.放电时正极附近溶液的碱性增强 |
| B.放电时每转移3 mol电子,正极有1mol K2FeO4被还原 |
| C.充电时锌极与外电源负极相连 |
| D.充电时阳极反应为:Fe(OH)3- 3e- + H2O |
COCl2(g) CO(g)+ Cl2(g)△H>0。当反应达到平衡时,下列措施:①升温②恒容通入惰性气体③增加CO的浓度④减压⑤加催化剂⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+ Cl2(g)△H>0。当反应达到平衡时,下列措施:①升温②恒容通入惰性气体③增加CO的浓度④减压⑤加催化剂⑥恒压通入惰性气体,能提高COCl2转化率的是
| A.①②④ | B.②③⑥ | C.①④⑥ | D.③⑤⑥ |