欲配制100ml 1.0 mol/L Na2SO4溶液,正确的方法是
① 将14.2 g Na2SO4 溶于100ml水中
② 将32.2g Na2SO4·10H2O溶于少量水中,再用水稀释至100 ml
③ 将20 ml 5.0 mol/L Na2SO4溶液用水稀释至100 ml
| A.①② | B.②③ | C.①③ | D.①②③ |
⑴ 由钛铁矿(FeTiO3)提取金属钛(海绵钛)的主要工艺过程如下(部分产物省略):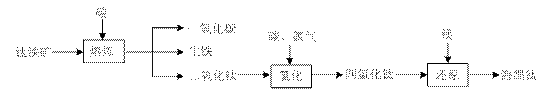
上述熔炼过程发生的反应为吸热反应,该反应能够自发进行的原因是▲;还原过程必须在1070K的温度下进行,你认为还应该控制的反应条件是▲。
⑵ 用浓硫酸处理钛铁矿,并向所得溶液中加入铁,此时溶液中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
| 氢氧化物 |
Fe(OH)2 |
TiO(OH)2 |
Mg(OH)2 |
| Ksp |
8.0×10-16 |
1.0×10-29 |
1.8×10-11 |
常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol/L,当溶液的pH等于▲时,Mg(OH)2开始沉淀。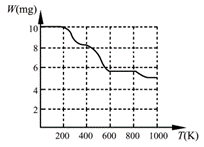 若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量
若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量
白色沉淀,写出该反应的离子方程式:▲。
⑶ BaTiO3是一种可用来吸收低频波的无机功能材料。工业上,常用
BaCl2、TiCl4、H2O和H2C2O4混合反应生成白色固体A,将该白色
固体加热分解至900K可得BaTiO3,实验测得其热分解过程的质量
-温度关系曲线如右图所示,图中400K、600K和900K时对应的
样品的质量分别为8.38mg、5.68mg和5.19mg。白色固体A的化学式
为▲(填序号)。
a.BaTi2O5b.BaC2O4·2H2Oc.BaTi(C2O4)3d.BaTiO (C2O4)2·4H2O
 |
请回答下列问题:
⑴ G的化学式为▲。
⑵ 写出B与C反应的化学方程式▲。
⑶ J、K是同种金属的氯化物,且K为白色沉淀。写出SO2还原J生成K的离子方程式▲。
⑷ 汽车尾气中常含有D。B与D在加热和催化剂存在的条件下,发生反应生成两种对空气无污染的物质。请写出该反应的化学方程式▲。
| A.0.2 mol/L的NaHCO3溶液: c(HCO3-)>c(CO32-)>0.1 mol/L>c(H2CO3) |
| B.pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合: c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| C.0.2 mol/L CH3COOH溶液和0.2 mol/L CH3COONa溶液等体积混合: c(CH3COO-)+c(OH-)-c(H+)=0.1 mol/L |
| D.0.1mol/LNa2CO3溶液与0.1mol/LNaHCO3溶液等体积混合 |
c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+)
| A.pH=2的溶液:Fe3+、Cu2+、SO42-、NO3- |
| B.c(H+)=1×10-12mol/L的溶液:NH4+、K+、Cl-、AlO2- |
| C.水电离的c(H+)=1×10-12mol/L的溶液:Na+、Al3+、Br-、ClO- |
| D.与铝反应放出氢气的溶液:Na+、Mg2+、Br-、Cl- |