Na2FeO4是一种高效多功能水处理剂,应用前景广阔,一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2==2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法不正确的是
| A.Na2O2在反应中只作氧化剂 |
| B.O2是氧化产物 |
| C.Na2FeO4既是氧化产物又是还原产物 |
| D.2 mol FeSO4发生反应时,共有10 mol电子转移 |
如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是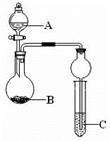
| A.若A为浓硝酸,B为金属铜,C中盛有淀粉KI溶液,则C中溶液变蓝 |
| B.若A为浓盐酸,B为MnO2,C中盛石蕊试液,则C中溶液先变红后褪色 |
| C.若A为浓氨水,B为生石灰,C中盛A1C13溶液,则C中产生白色沉淀 |
| D.若A为浓硫酸,B为炭,C中盛有品红溶液,则C中溶液红色褪色 |
下列离子方程式正确的是
| A.向氯化铝溶液中加入过量氨水:Al3++4OH-=AlO2—+2H2O |
| B.金属钠与水反应: Na+H2O=Na++OH-+ H2↑ |
| C.Ba(OH)2溶液中滴加少量NH4HCO3溶液:NH4++HCO3-+2OH-+Ba2+=NH3·H2O+H2O+BaCO3↓ |
D.用铁棒作阴极、炭棒作阳极电解饱和氯化钠溶液:2C1-+2H2O  H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn + 2K2FeO4 + 8H2O 3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述不正确的是
3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述不正确的是
| A.放电时K+ 向负极移动 |
| B.放电时负极区域的pH会增大 |
| C.充电时锌极与外电源负极相连 |
| D.充电时阳极反应为:Fe(OH)3-3e- + 5OH-="===" FeO42- + 4H2O |
国庆期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开。S-诱抗素的分子结构如右图,下列关于该物质的说法正确的是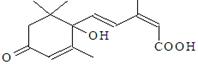
| A.其分子式为C15H21O4 |
| B.分子中只含有1个手性碳原子 |
| C.既能发生加聚反应,又能发生缩聚反应 |
| D.既能与FeCl3溶液发生显色反应,又能使酸性KMnO4溶液褪色 |
一定条件下,用甲烷可以消除氮的氧化物(NOx)的污染。已知:
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160 kJ·mol-1
下列选项正确的是
| A.CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1 |
| B.CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(g) ΔH=+1734 kJ·mol-1 |
| C.CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(l)ΔH=-x kJ·mol-1 x <574 |
| D.常温常压下用2.24 L CH4还原NO2至N2,整个过程中转移的电子为0.8 mol |