阿伏加德罗常数的值约为6.02×1023mol-1,下列叙述中不正确的是( )
①12.4g白磷晶体中含有的P-P键数约是0.6×6.02×1023
②0.5 mol·L—1 Mg(NO3) 2溶液中含有NO 的数目为2NA
的数目为2NA
③7.8 g Na2S和Na2O2的混合物中含有的阴离子数大于0.1×6.02×1023
④2mol SO2和1 mol O2混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2×6.02×1023
⑤Fe与0.1 mol氯气反应时失去的电子数为0.3 NA
⑥含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA
| A.① ④ ⑥ | B.① ③ ④ ⑤ ⑥ | C.② ③ ⑤ ⑥ | D.③ ④ ⑤ ⑥ |
下列有机物命名正确的是
A.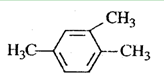 1,3,4-三甲苯 1,3,4-三甲苯 |
B.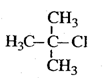 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 |
C.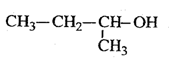 2-甲基-1-丙醇 2-甲基-1-丙醇 |
D.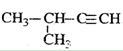 2-甲基-3-丁炔 2-甲基-3-丁炔 |
下列对有机物结构或性质的描述,错误的是
| A.一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应 |
| B.苯酚钠溶液中通入CO2生成苯酚,则碳酸的酸性比苯酚弱 |
| C.乙烷和丙烯的物质的量各1mol,完成燃烧生成3molH2O |
| D.光照下2,2—二甲基丙烷与Br2反应其一溴取代物只有一种 |
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是
| A.含有碳碳双键、羟基、羰基、羧基 |
| B.含有苯环、羟基、羰基、羧基 |
| C.含有羟基、羰基、羧基、酯基 |
| D.含有碳碳双键、苯环、羟基、羰基 |
下列关于有机物的说法错误的是
| A.CCl4可由CH4制得,可萃取碘水中的碘 |
| B.石油和天然气的主要成分都是碳氢化合物 |
| C.乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 |
| D.苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 |
下列各组有机物只用一种试剂无法鉴别的是
| A.乙醇、甲苯、硝基苯 | B.苯、苯酚、己烯 |
| C.苯、甲苯、环己烷 | D.甲酸、乙醛、乙酸 |