高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为,下列叙述不正确的是
| A.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化 |
B.充电时阳极反应为:Fe(OH)3—3e— + 5 OH—= FeO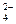 + 4H2O + 4H2O |
| C.放电时负极反应为:Zn—2e— +2OH—= Zn(OH)2 |
| D.放电时正极附近溶液的碱性增强 |
等量的镁铝合金粉末分别与下列4种过量的溶液充分反应,放出氢气最多的是
| A.2 mol·L-1H2SO4溶液 |
| B.3 mol·L-1CuSO4溶液 |
| C.6 mol·L-1KOH溶液 |
| D.3 mol·L-1Ba(OH)2溶液 |
将等物质的量的金属Na、Mg、Al分别与100 mL 2 mol·L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如图所示,则下列说法错误的是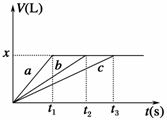
| A.x=2.24 |
| B.钠的物质的量为0.2 mol |
| C.反应时,Na、Mg、Al均过量 |
| D.曲线b为Mg与盐酸反应的图像 |
由锌、铁、铝、镁四种金属中的两种组成的混合物10 g,与足量的盐酸反应产生的氢气在标准状况下为11.2 L,则混合物中一定含有的金属是
| A.锌 | B.铁 | C.铝 | D.镁 |
Mg、Al两种金属分别跟相同体积、相同浓度的稀H2SO4反应,同温同压下生成氢气的体积相同,则Mg、Al两种金属之间的量的关系一定正确的是
| A.两个反应转移的电子数目相等 |
| B.加入镁、铝的质量比为4:3 |
| C.金属溶解的物质的量相等 |
| D.加入的两种金属的质量不等 |
下列反应中,硝酸既表现酸性,又表现氧化性的是
| A.Fe2O3跟稀硝酸反应 |
| B.铜跟稀硝酸反应 |
| C.CuO跟稀硝酸反应 |
| D.Al(OH)3跟稀硝酸反应 |