用惰性电极电解Fe2(SO4)3和CuSO4的混合溶液,下列说法正确的是
| A.阴极反应式为:Cu2++2e—====Cu,当有Cu2+存在时,Fe3+不放电 |
| B.阴极上首先析出铁,然后析出铜 |
| C.阴极先是Fe3+放电,后Cu2+放电 |
| D.阴极上不可能析出铜 |
一定条件下,可逆反应C(s)+CO2(g)  2CO(g) ΔH<0,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积:④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是( )
2CO(g) ΔH<0,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积:④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是( )
| A.①②③④ | B.①③ | C.④② | D.①③④ |
对于可逆反应 A(g) +2B(g) 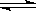 2C(g)ΔH>0,反应时间t,温度T与平衡混合物中
2C(g)ΔH>0,反应时间t,温度T与平衡混合物中
C的百分含量关系的是()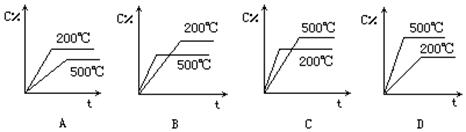
对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述中正确的是( )
4NO(g)+6H2O(g),下列叙述中正确的是( )
| A.达到化学平衡时4v正(O2)=5v逆(NO) |
| B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
| C.达到化学平衡时,若增大容器的体积,则正反应速率减小,逆反应速率增大 |
| D.化学反应速率的关系是2v正(NH3)=3v正(H2O) |
下列化学实验事实及解释都正确的是 ()
| A.碳酸钙不溶于水,所以它是非电解质 |
| B.强电解质的水溶液一定比弱电解质溶液的导电能力强 |
| C.升高温度可以增大单位体积内活化分子的百分数 |
| D.非自发反应在任何条件下都不能实现 |
下列物质在水溶液中的电离方程式书写正确的是()
| A.CH3COOH ="=" H++CH3COO- | B.Na2SO4=== 2Na++SO42- |
C.H2S 2H++ S2- 2H++ S2- |
D.NaHCO3 Na++H++CO Na++H++CO |