海水中溶解和悬浮着大量的无机物与有机物,具有巨大的开发潜力,人类除了从海水中获得食盐和水外,还获得大量的钾、镁、溴、碘等,以下说法不正确的是 ( )
| A.钾与溴两种元素位于周期表中同一周期,二者形成的化合物中只有离子键 |
| B.轮船在海水中与在江河中航行相比,在海水中更易被腐蚀 |
C.若氯有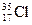 、 、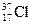 两种核素,则 两种核素,则 、 、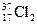 化学性质几乎相同 化学性质几乎相同 |
| D.海水中的上述元素变成单质状态过程中,均发生了氧化反应 |
一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3=2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为()
| A.5∶3 | B.5∶4 | C.1∶1 | D.3∶5 |
下列离子方程式与所述事实相符且正确的是()
| A.铝粉投入到NaOH溶液中:2Al+2OH-= 2AlO2-+H2↑ |
B.AlCl3溶液中加入足量的氨水:Al3++ 3 OH- = Al(OH)3↓ Al(OH)3↓ |
| C.工业制漂白液:Cl2+2OH-=ClO-+Cl- +H2O |
| D.FeCl3溶液跟Cu反应:2Fe3++Cu=2Fe+Cu2+ |
实现下列变化需要加入还原剂才能实现的是()
A.Fe2O3 →FeB .Cu →Cu(NO3)2C.SO3→ H2SO4D.Cl2→Cl-
.Cu →Cu(NO3)2C.SO3→ H2SO4D.Cl2→Cl-
设NA为阿伏伽德罗常数,下列叙述正确的是:()
| A.18 g重水(D2O)中所含电子数为10 NA |
| B.在25 ℃,1.013×105 Pa条件下,11.2 L氯气所含原子数为 NA个 |
| C.常温常压下,32 g氧气中含有2 NA个氧原子 |
| D.32 g S8单质中含有的S—S键个数为12.04×1023 |
下列事实或变化,能证明一水合氨是弱电解质的是()
| A.氨水受热分解挥发出氨气 |
B.氨水与醋 酸反应生成醋酸铵,而醋酸铵是强电解质 酸反应生成醋酸铵,而醋酸铵是强电解质 |
| C.氨水的导电能力弱 |
| D.在氨水溶液中存在NH3·H2O分子 |