纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。
制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗除去其中的Cl,再烘干、焙烧除去水分得到粉体TiO2 。
用现代分析仪器测定TiO2粒子的大小。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
⑴ TiCl4水解生成TiO2·xH2O的化学方程式为 ▲ 。
⑵ 检验TiO2·xH2O中Cl-是否被洗净的方法是 ▲ 。
⑶配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是 ▲ ;使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的 ▲(填字母代号)。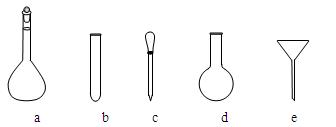
⑷滴定终点的现象是 ▲ 。
⑸滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样w g,消耗c mol·L-1 NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为 ▲ 。
⑹判断下列操作对TiO2质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”)
① 若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,使测定结果 ▲ 。
② 若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果 ▲
感冒是一种常见的病,人患了感冒会咳嗽、流涕、发烧,多喝开水多休息,适当服用一些治疗感冒的药,可以舒缓症状,减轻病情。
(1)药物阿司匹林是一种传统的治疗感冒发烧的老药,从分子结构上看,它可以看作是乙酸酯,其结构简式如右图: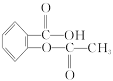
作为一种解热镇痛药,对于感冒发烧,它有较好的疗效,但大剂量长期空腹服用,容易对胃肠道产生刺激,原因是阿司匹林在胃中会发生酯的水解反应,生成_________和_________(用结构简式表示),阿司匹林分子水解后,能电离出氢离子(H+)的官能团增多,增大了对胃肠道的刺激。
(2)为减小副作用,一般宜饭后服药,并同时服用少量辅助药物,在①硫酸镁、②氢氧化钡、③碳酸钙中选取哪一种?
某学生欲测定味精中食盐的含量,做了如下实验:
①称取某牌号的袋装味精样品1.0 g;②将样品溶于适量蒸馏水中,加入足量用稀硝酸酸化的A溶液,充分反应,使沉淀完全;③过滤,并用蒸馏水洗涤沉淀多次;④将沉淀烘干称量,测得固体质量为0.50 g。
根据上述实验操作回答下列问题:
(1)加入的A溶液是__________;检验加入的A是否过量的方法是____________________。
(2)过滤时,为提高过滤效率,可用如右图所示的装置(称为抽滤装置)代替普通过滤装置,抽滤装置过滤速率比普通过滤装置快的主要原因是___________________________________。
(3)洗涤沉淀的方法____________________________________________________________。
(4)烘干沉淀应采用的方法是__________。
A.低温烘干 B.高温烘干 C.利用太阳能晒干
(5)该牌号味精中氯化钠的质量分数为__________,若该味精包装袋上标注“谷氨酸单钠含量≥80%,NaCl含量≤20%”,则此样品是否符合产品标示的质量分数__________(填“符合”或“不符合)。
味精是烹制菜肴时常用的调味品,其主要成分是谷氨酸钠(化学式为C5H8NO4Na)。谷氨酸钠有鲜味,易溶于水。某品牌味精包装上标注:“谷氨酸钠含量≥80%,NaCl含量<20%”。
某学校化学科研小组对此味精中NaCl的含量进行测定。
Ⅰ.查阅资料:谷氨酸钠的存在不影响NaCl含量的测定。
Ⅱ.设计实验方案:
(1)实验原理:通过味精与硝酸银反应生成氯化银的质量计算该味精中NaCl的质量分数。
(2)实验试剂:水、AgNO3溶液等
(3)实验过程: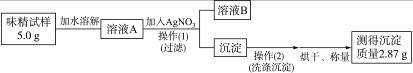
①操作(Ⅰ)所需要的玻璃仪器有____________________。
②通过计算判断该味精中NaCl的质量分数是__________,判断该味精中NaCl __________(填“符合”或“不符合”)其包装上标注的标准。
③若溶液A的体积为50 mL,则其中NaCl的物质的量浓度为____________________。
分别取1 mol葡萄糖进行下列实验:
(1)与银氨溶液发生银镜反应,能还原得到__________ mol银单质,反应后葡萄糖变为(结构简式)__________。
(2)与醋酸发生酯化反应,需__________ g醋酸才能完全酯化。
(3)若使之完全转化为H2O和CO2,所需O2的体积(标准状况)为__________ L。
(4)与新制Cu(OH)2悬浊液反应的化学方程式为_________________________________。
某酒厂所生产的啤酒、果子酒放置久了会产生沉淀,从而影响销售造成产品积压。经化验,得知沉淀物是蛋白质,为了解决这一问题,提出了两种方案:
甲:在酒中加入少量蛋白酶(可使蛋白质水解的生物催化剂);
乙:在酒中加入少量氨基酸氧化酶(可使氨基酸氧化的生物催化剂)。
(注:酶具有专一性,即一种酶只能催化一种物质反应)
请评价这两种方案:
①__________方案合理,原因是___________________________________________________。
②__________方案不合理,原因是_________________________________________________。