在0.1mol·L-1 CH3COOH溶液中存在如下电离平衡:CH3COOH  CH3COO-+H+,对于该平衡,下列叙述中,正确的是
CH3COO-+H+,对于该平衡,下列叙述中,正确的是
| A.加入水时,平衡向逆反应方向移动 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.加入少量0.1 mol·L-1 HCl溶液,溶液中[ H+] 减小 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
除去下列物质中所含少量杂质的方法正确的是
| 物质 |
杂质 |
试剂 |
提纯方法 |
|
| A |
BaSO4 |
BaCO3 |
稀盐酸 |
溶解、过滤、洗涤 |
| B |
CO2 |
SO2 |
饱和Na2CO3溶液 |
洗气 |
| C |
乙酸乙酯 |
乙酸 |
稀NaOH溶液 |
混合振荡、静置分液 |
| D |
蛋白质 |
蔗糖 |
浓(NH4)SO4溶液 |
盐析、过滤、洗涤 |
25℃时,某硫酸铜溶液的质量分数为w,物质的量浓度为cmol/L,密度为ρg/mL,将此溶液蒸去a g水或再向原溶液中加入b g无水硫酸铜粉末,充分静置并恢复至25℃时,均恰好全部转化为CuSO4·5H2O晶体。则下列关系式正确的是
A.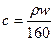 |
B.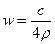 |
C.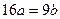 |
D. |
阿伏加德罗常数约为6.02×1023mol-1,下列叙述中正确的是
| A.0.5g C3H4中含有共用电子对的数目为0.1×6.02×1023 |
| B.3.0 g淀粉和葡萄糖混合物中共含碳原子数为0.1×6.02×1023 |
| C.25℃时pH=1的醋酸溶液中含有H+的数目为0.1×6.02×1023 |
| D.标准状况下,2.24L CHCl3含有的分子数为0.1×6.02×1023 |
下列实验操作正确的是
| A.用100mL容量瓶准确量取100mL溶液 |
| B.中和滴定前,锥形瓶用蒸馏水荡洗后直接装入待测液 |
| C.用稀硫酸洗涤久置石灰水的试剂瓶 |
| D.用pH试纸蘸取稀盐酸,取出与标准比色卡对比 |
25℃时,在含有大量Ba2+的某澄清透明溶液中,由水电离产生的OH-物质的量浓度为1×10-12mol/L,则在此溶液中还可能大量共存的离子组有
| A.Na+、Fe2+、NO3- | B.K+、CH3COO-、SO42- |
| C.NH4+、HCO3-、SCN- | D.Cu2+、Mg2+、Cl- |