下图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充、放电的化学方程式为:2K2S2+KI3 K2S4+3KI。装置(Ⅱ)为电解池的示意图。当闭合开关K时,X附近溶液先变红。则下列说法正确的是( )
K2S4+3KI。装置(Ⅱ)为电解池的示意图。当闭合开关K时,X附近溶液先变红。则下列说法正确的是( )
| A.闭合K时,K+从右到左通过离子交换膜 |
| B.闭合K时,A的电极反应式为:3I--2e-===I |
| C.闭合K时,X的电极反应式为:2Cl--2e-===Cl2↑ |
| D.闭合K时,当有0.1 mol K+通过离子交换膜,X电极上产生标准状况下气体1.12 L |
某同学利用下图所示装置进行实验,一段时间后,水沿导管缓慢上升,下列说法正确的是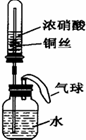
| A.实验过程中气球体积不会发生变化 |
| B.广口瓶内中液体的pH值增大 |
| C.广口瓶中有化合反应发生 |
| D.试管中不可能发生分解反应 |
往NH4Cl溶液加入少量Na2O固体,溶液中颗粒的数目不变的是
| A.NH4+ | B.H+ | C.Cl- | D.H2O |
下列关于有机化合物的说法不正确的是
| A.乙烯和甲烷可用溴的四氯化碳溶液鉴别 |
| B.乙酸可与NaHCO3溶液反应生成CO2 |
| C.蛋白质和油脂在一定条件下都能水解 |
| D.葡萄糖和麦芽糖互为同系物 |
化学与社会、生产、生活紧切相关,下列说法正确的是
| A.医疗上可用硫酸钡作x射线透视肠胃的内服药,是因为硫酸钡不溶于水 |
| B.酸雨指25℃时pH值小于7的降水 |
| C.加碘食盐中添加碘酸钾而不用碘化钾,是因为碘酸钾能溶于水而碘化钾不溶于水 |
| D.发酵粉能使焙制出的糕点疏松多孔,是因为发酵粉中含有碳酸氢钠 |
X、Y、Z、W为原子序数依次增大的短周期元素。其形成的小分子化合物Y2X2、Z2X4、X2W2中,相应分子内各原子最外层电子都满足稳定结构。下列说法正确的是
| A.X、Y、Z、W的原子半径的大小关系为:W> Y >Z> X |
| B.在化合物Y2X2、Z2X4、X2W2中,分子所含的共用电子对数相等 |
| C.与元素Y、Z相比,元素W形成的简单氢化物最稳定,是因为其分子间存在氢键 |
| D.X、Y、Z、W四种元素可形成化学式为X7Y2ZW2的有机物 |