 向体积为Va的0.05mol·L-1CH3COOH溶液中加入体积为Vb的0.05mol·L-1KOH溶液,下列关系错误的是
向体积为Va的0.05mol·L-1CH3COOH溶液中加入体积为Vb的0.05mol·L-1KOH溶液,下列关系错误的是
A.Va>Vb时:c (CH3COOH) +c (CH3COO-)>c (K+) |
B.Va=Vb时:c (CH3COOH) +c (H+)>c (OH-) |
C.Va<Vb时:c (CH3COO-)>c (K+)> c (OH-)> c (H) |
D.Va与Vb任意比时:c (K+)+ c (H+)=c (OH-)+ c (CH3COO-) |
研究发现CuSO4和FeS2在一定条件下可发生如下反应:14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4;下列说法正确的是
| A.FeS2中的硫元素全部被氧化 |
| B.5 mol FeS2发生反应,有10 mol电子转移 |
| C.产物中SO42-有一部分是氧化产物 |
| D.FeS2只用作还原剂 |
向FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是
| A.加入KSCN溶液一定不变红色 | B.溶液中一定含Fe2+ |
| C.溶液中一定含Cu2+ | D.剩余固体中一定含Cu |
下列关于氧化性、还原性的判断正确的是
| A.B的阳离子的氧化性比A的阳离子强,说明A元素的金属性一定比B元素强 |
| B.发生氧化还原反应时A原子失去的电子比B原子多,证明A的金属性一定比B强 |
| C.适量的Cl2通入FeI2溶液中可发生反应:3Cl2+6FeI2=2FeCl3+4FeI3 |
| D.一定量氯气通入30 mL 10.00 mol·L-1的氢氧化钠溶液中,加热后形成NaCl、NaClO、NaClO3共存的溶液,若反应中转移的电子为n mol,则0.15<n<0.25 |
有一无色溶液,可能含有Fe3+、K+、Al3+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量的Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是
| A.肯定有Al3+、Mg2+、NH4+、Cl- | B.肯定有Al3+、Mg2+、HCO3- |
| C.肯定有K+、HCO3-、MnO4- | D.肯定有Al3+、Mg2+、SO42- |
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是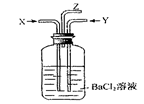
| A.洗气瓶中产生的沉淀是BaCO3 |
| B.在Z导管出来的气体中无CO2 |
| C.洗气瓶中产生的沉淀是BaSO3 |
| D.在Z导管口有红棕色气体出现 |