下列离子方程式正确的是 ( )
| A.用稀氢氧化钠溶液吸收二氧化氮:2OH-+3NO2=2NO3-+NO↑+H2O |
B.等体积、等浓度的Ca(HCO3)2溶液和NaOH溶液混合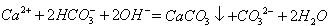 |
| C.Na2O2与H2O反应制备O2:Na2O2 + H2O= 2Na+ + 2OH- + O2↑ |
D.苯酚与碳酸钠溶液的反应: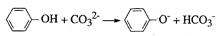 |
用以下三种途径来制取相等质量的硝酸铜:(1)铜跟浓硝酸反应;(2)铜跟稀硝酸反应;(3)铜先跟氧气反应生成氧化铜,氧化铜再跟硝酸反应。以下叙述中正确的是()
| A.三种途径所消耗的铜的物质的量相等 |
| B.三种途径所消耗的硝酸的物质的量相等 |
| C.所消耗的铜的物质的量是:途径(3)>途径(1)>途径(2) |
| D.所消耗的硝酸的物质的量是:途径(1)>途径(2)>途径(3) |
下列离子方程式正确的是()
| A.高锰酸钾与浓盐酸反应:2 MnO4- + 10 Cl- + 16 H+ =" 2" Mn2+ + 5 Cl2↑ + 8 H2O |
| B.标准状况112 mLCl2通入10 mL 1mol/LFeBr2溶液:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 |
C.浓盐酸和KClO3反应: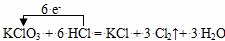 |
| D.硫化钠溶于水显碱性:S2- + 2H2O = H2S + 2OH- |
实验是化学研究的基础,下图中所示的实验方法、装置或操作完全正确的是()
下列排列顺序正确的是()
①热稳定性:H2O>HF>H2S②原子半径:Na>Mg>O
③电负性:Cl>P>S④结合质子能力:OH->CH3COO->Cl-
| A.①③ | B.②④ | C.①④ | D.②③ |
下列各溶液中一定能大量共存的离子组是()
| A.加入铝粉有氢气生成的溶液中:Mg2+、Cu2+、SO42-、K+ |
| B.在c(Fe3+)=0.1mol· L-1的溶液中:K+、ClO-、SO42-、SCN- |
| C.c(H+)=10-14mol/L的溶液中:Na+、AlO2-、S2-、SO32- |
| D.水电离出的c(H+)与c(OH-)乘积为10-28的溶液中:Ca2+、Na+、HCO3-、K+ |