已知:t℃下的某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为: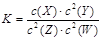 ,有关该平衡的说法中正确的是( )
,有关该平衡的说法中正确的是( )
| A.升高温度,平衡常数K变大 |
| B.增大压强,W(g)物质的量分数变小 |
| C.升温,若混合气体的平均相对分子质量变小,则逆反应放热 |
| D.增大Z浓度,平衡向正反应方向移动 |
下列反应属于放热反应的是
| A.氢氧化钡晶体和氯化铵晶体的反应 |
| B.能量变化如图所示的反应 |
| C.化学键断裂吸收的热量比化学键生成放出的热量多的反应 |
| D.燃烧反应和中和反应 |
自瑞士ETH天文研究所的Ansgar Grimberg等的研究结果表明,太阳气体中存在大量的20Ne和22Ne。下列关于20Ne和22Ne的说法正确的是
| A.20Ne和22Ne互为同位素 | B.20Ne和22Ne是同一种核素 |
| C.20Ne的原子核中有20个质子 | D.22Ne的原子核中有22个中子 |
科学家发现C60后,近年又合成了许多球形分子(富勒烯),如C50、C70、C120、C540等,它们互称为
| A.同种物质 | B.同分异构体 | C.同素异形体 | D.同位素 |
新能源的开发利用是人类社会可持续发展的重要课题。下列属于新能源的是
| A.氢气 | B.煤炭 | C.天然气 | D.石油 |
根据四种变化:①Fe(s)→Fe(g);②2H2(g)+ O2(g)=2H2O(g) △H="-482" kJ·mol-1;
③C(s)+CO2(g)=2CO(g);④NaOH(s)=Na+(aq)+OH-(aq)。请回答下列问题
⑴上述变化中,需要吸收热量的是(请填变化的代码①②③④,下同)。
⑵上述变化中,体系的混乱度增大的是。
⑶已知下列两种键能,H-H:436 kJ·mol-1、O-H:463 kJ·mol-1,请计算断裂1 molO2(g)中的共价键需要吸收kJ的能量。
⑷下面几种说法中。正确的是[
| A.化合反应都大多是放热反应 |
| B.凡是需要加热的反应,都是吸热反应 |
| C.体系的混乱度增大的反应都是吸热反应 |
| D.中和反应是放热反应,其化学能可以转化成电能 |