北京大学和中国科学院的化学工作者已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子晶体,具有良好的超导性。下列有关分析正确的是( )
| A.K3C60中既有离子键,又有极性键 | B.K3C60中碳元素显-3价 |
| C.该晶体在熔融状态下能导电 | D.C60与C—12互为同素异形体 |
将浓HCl、浓HNO3、浓H2SO4分别滴在三张蓝色的石蕊试纸上,片刻后可观察到三张试纸的颜色是()
| A.红、黑、红 | B.红、蓝、黑 |
| C.红、白、黑 | D.红、红、红 |
如右图所示,红磷和硫在集气瓶中燃烧,当火焰熄灭后,同时打开两个止水夹,可以观察到的现象是()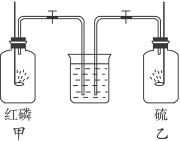
| A.水迅速进入甲瓶和乙瓶 |
| B.水都不进入甲、乙两瓶 |
| C.水只进入甲瓶而不进入乙瓶 |
| D.水只进入乙瓶而不进入甲瓶 |
除去试管内附着的银,最好选用()
| A.浓HNO3 | B.稀HNO3 |
| C.稀HCl | D.稀氨水 |
14 mL二氧化氮和氨的混合气体在一定条件下充分反应,化学方程式是6NO2+8NH3====7N2+12H2O。已知该混合气体参加反应的二氧化氮比参加反应的氨少2 mL(气体体积均在相同状况下测定),则原混合气体中二氧化氮和氨的物质的量之比是()
| A.3∶2 | B.2∶3 |
| C.3∶7 | D.3∶4 |
工业上用焦炭、水、空气为原料制NH3时,有关反应如下:C+H2O(g) CO+H2;CO+H2O(g)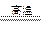 CO2+H2;N2+3H2
CO2+H2;N2+3H2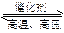 2NH3。根据化学方程式可知,理论上C与NH3的物质的量之比是()
2NH3。根据化学方程式可知,理论上C与NH3的物质的量之比是()
| A.2∶3 | B.3∶2 |
| C.4∶3 | D.3∶4 |