将纯水加热至较高温度,下列叙述正确的是
| A.水的离子积变大、pH变小、呈酸性 | B.水的离子积不变、pH不变、呈中性 |
| C.水的离子积变小、pH变大、呈碱性 | D.水的离子积变大、pH变小、呈中性 |
氯化铁溶液与氢氧化铁胶体具有的共同性质是
| A.分散质粒子直径都在1~100nm之间 |
| B.均能产生丁达尔效应 |
| C.用漏斗过滤时滤纸上没有滤渣留下 |
| D.均呈红褐色 |
下列有关物质组成的说法正确的是
| A.物质均是由分子构成,分子均是由原子构成 |
| B.某物质经测定,只含有一种组成元素,则该物质一定是单质 |
| C.碱性氧化物均是金属氧化物,酸性氧化物均是非金属氧化物 |
| D.纯净的硫酸是纯净物,而纯净的盐酸是混合物 |
下列各图所示装置,肯定不符合气密性要求的是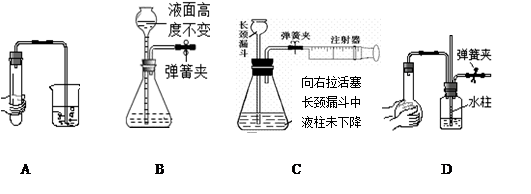
氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于区域3的是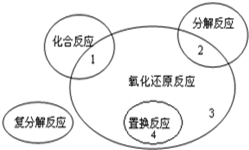
| A.2F2+2H2O═4HF+O2 |
| B.AgNO3+NaCl═AgCl↓+NaNO3 |
C.3CO+Fe2O3  2Fe+3CO2 2Fe+3CO2 |
D.MgCl2(熔融)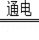 Mg+Cl2↑ Mg+Cl2↑ |
常温下,某100 mL溶液中含H2SO4 0.50 mol,加入下列物质,使溶液的导电性增强的是
| A.0.50 mol Ba(OH)2 |
| B.100 mL水 |
| C.0.50 mol酒精 |
| D.0.50 mol Na2SO4 |