在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察下图,然后回答问题。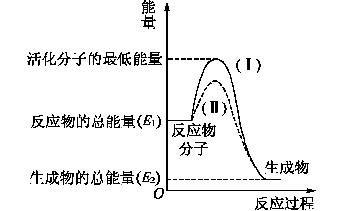
(1)图中所示的反应是__________(填“吸热”或“放热”)反应,该反应________(填“需要”或“不需要” )加热,该反应的ΔH=________(用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ/mol,该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为__________。
(3)对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子百分数增多,反应速率加快,你认为最可能的原因___________。
⑴乙醇的分子结构
结构式:
结构简式:
⑵、乙醇的化学性质
①乙醇能与金属钠(活泼的金属)反应:
并完成下表。
|
金属钠 的变化 |
气体燃 烧现象 |
检验 产物 |
||||||||
| 水 |
|||||||||||
| 乙醇 |
②醇的氧化反应
乙醇燃烧化学反应方程式:
乙醇在Cu做催化剂时加热的化学方程式:
平达喜是常用的中和胃酸的药物,它的化学成分是铝和镁的碱式碳酸盐,其中氢元素的质量分数为0.040。取该碱式盐3.01g,加入2.0mol·L-1盐酸使其溶解,当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全。若在上述碱式盐溶于盐酸后的溶液中加入过量的氢氧化钠,过滤,沉淀物进行干燥后重1.74g。试通过计算推测该碱式盐的化学式。
某有机物组成中含碳54.5%, 含氢9.1%,其余为氧,又知其蒸汽在标准状况下的密度为3.94 g/L,试求其分子式。
在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
图中: ① 为氯气发生装置;②的试管里盛有15mL30%KOH 溶液,并置于热水浴中; ③ 的试管里盛有15mL 8 % NaOH 溶液,并置于冰水浴中; ④ 的试管里加有紫色石蕊试液; ⑤ 为尾气吸收装置。
请填写下列空白:
(l)制取氯气时,在烧瓶里加入一定量的二氧化锰。通过_______________________
(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有_____________________(填写下列编号字母)的净化装置。
| A.碱石灰 | B.饱和食盐水 | C.浓硫酸 | D.饱和碳酸氢钠溶液 |
(2)比较制取氯酸钾和次氯酸钠的条件。二者的差异是: ___________________________
反应完毕经冷却后,② 的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是_________________(填写编号字母);从②的试管中分离出该晶体的方法是__________(填写实验操作名称)。
(3)本实验中制取次氯酸钠的离子方程式_______________________ 。
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
| 实验现象 |
原因 |
| 溶液最初从紫色逐渐变为____色 |
氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 |
|
| 然后溶液从无色逐渐变为____色 |
碱式碳酸镁有多种不同的组成,如 、
、 、
、 等。请你设计一个测定碱式碳酸镁组成的实验方案。包括
等。请你设计一个测定碱式碳酸镁组成的实验方案。包括
(1)测定原理
(2)测定实验的装置图
(3)操作步骤。
可使用的仪器、试剂和用品如下:
仪器:天平(附砝码)、大试管(附带有短玻璃管的橡皮塞)、酒精灯、洗气瓶、球形干燥管(附带有短玻璃管的橡皮塞)、铁架台、铁夹、角匙。
试剂:碱式碳酸镁(粉状)、浓硫酸、石灰水、无水氯化钙、碱石灰。
其他:火柴、棉花、短橡皮管、弹簧夹。
注意:①上述仪器和试剂只需应用其中的一部分。②仪器、试剂、用品的数量不限。