下列物质中所含分子物质的量最多的是
| A.56gN2 | B.1.5molO2 |
| C.标准状态下22.4LCl2 | D.3.01×1023个硫酸分子 |
下列各组离子能在水溶液中大量共存的是
| A.H+、Fe2+、ClO-、SO42- | B.Na+、Cu2+、S2-、ClO- |
| C.Na+、Ba2+、OH-、NO3- | D.Na+、Al3+、SiO32-、CO32- |
下列关于有机物的说法正确的是
| A.涤纶、纤维素、酚醛树脂都是合成材料 |
| B.汽油和植物油都是混合物,主要成份是烃和酯 |
| C.甲酸与乙酸是有机酸,都不能被酸性高锰酸钾溶液氧化 |
| D.葡萄糖、蔗糖、淀粉在一定条件下都可发生水解反应 |
下列变化过程,属于放热过程的是
| A.酸碱中和反应 | B.液态水变成水蒸气 |
| C.弱酸弱碱电离 | D.用FeCl3饱和溶液制Fe(OH)3胶体 |
下列实验结论正确的是
| 选项 |
实验操作 |
现象 |
结论 |
| A |
取待测液先进行焰色反应,再加足量稀盐酸,将产生气体通入品红溶液 |
火焰呈黄色,品红溶液褪色 |
原溶液一定是亚硫酸钠溶液 |
| B |
向浓醋酸溶液中加入少量碳酸钠溶液,将产生气体通入苯酚钠溶液 |
苯酚钠溶液中出现白色浑浊 |
不能说明酸性:醋酸>碳酸>苯酚 |
| C |
常温下向足量浓硫酸和稀硫酸中,分别加入相同质量、相同体积的铁片 |
相同时间两者产生H2速率不同 |
反应物的浓度越大,反应速率越快 |
| D |
相同的铝片分别与同温同体积,且c(H+)="1" mol·L¯1的盐酸、硫酸反应 |
铝与盐酸反应产生气泡较快 |
可能是Cl-对该反应起到促进作用 |
第二、三周期元素X、Y、Z、W与第四周期元素砷(33As)在周期表中的位置关系如下图所示,则下列说法中正确的是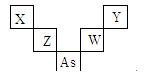
| A.Z的氧化物可与Y的氢化物水溶液发生化学反应 |
| B.X的原子半径比As原子半径小,两者原子序数之差为29 |
| C.W的氧化物对应的水化物是共价化合物,并且必是强酸 |
| D.图中五种元素均是非金属元素,并且Y的非金属性最强 |