0.035mol铜完全溶于硝酸,产生氮的氧化物(NO、NO2、N2O4)混合气体共0.05mol。该混合气体的平均相对分子质量可能是
| A.30 | B.42 | C.45 | D.60 |
某温度下的溶液中c(H+)=10xmol/L,c(OH-)=10ymol/L。x与y的关系图所示,下列说法正确的是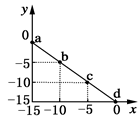
| A.该温度高于25℃ |
| B.图中a点溶液呈碱性 |
| C.该温度下,0.01 mol·L-1的HCl溶液的pH=2 |
| D.该温度下,0.01 mol·L-1的NaOH溶液的pH=12 |
蒸干下列溶液,能得到该溶质的是
| A.Na2SO3溶液 | B.KNO3溶液 | C.Fe2(SO4)3溶液 | D.AlCl3溶液 |
pH为3的CH3COOH和pH为11的NaOH溶液等体积混合,混合后溶液pH为()
| A.pH>7 | B.pH<7 | C.pH=7 | D.无法确定 |
某温度下,反应H2(g)+I2(g) 2HI(g)的正反应为放热反应,在带有活塞的密闭容器中达到平衡.下列说法中正确的是
2HI(g)的正反应为放热反应,在带有活塞的密闭容器中达到平衡.下列说法中正确的是
| A.体积不变,升温,正反应速率减小 |
| B.温度、压强均不变,充入HI气体,开始时正反应速率增大 |
| C.温度不变,压缩气体的体积,平衡不移动,颜色加深 |
| D.混和气体的密度不变,表示该反应达到平衡状态 |
已知下列热化学方程式:
①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l)ΔH1=-870.3 kJ/mol
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol
③H2(g)+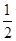 O2(g)===H2O(l) ΔH3=-285.8 kJ/mol
O2(g)===H2O(l) ΔH3=-285.8 kJ/mol
则反应④2C(s)+2H2(g)+O2(g)===CH3COOH(l)的焓变为
| A.488.3 kJ/mol | B.-224.15 kJ/mol |
| C.-488.3 kJ/mol | D.244.15 kJ/mol |