温度为T时,在2 L容积不变的密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积分数与时间的关系如图2所示。则下列结论错误的是
A.容器中发生的反应可表示为:3X(g)+Y(g) 2Z(g) 2Z(g) |
| B.保持其他条件不变,升高温度,平衡逆向移动 |
C.反应进行的前3min内,用X表示的反应速率 v(X ) =" 0.1" mol·L-1·min-1 ) =" 0.1" mol·L-1·min-1 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 |
某烯烃与H2加成后的产物是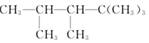 ,则该烯烃的结构式可能有
,则该烯烃的结构式可能有
| A.1种 | B.2种 | C.3种 | D.4种 |
有关烯烃的下列说法中正确的是
| A.烯烃分子中所有的原子一定在同一平面上 |
| B.烯烃在适宜的条件下只能发生加成反应不能发生取代反应 |
| C.分子式是C4H8的烃分子中一定含有碳碳双键 |
| D.烯烃既能使溴水褪色也能使酸性KMnO4溶液褪色 |
下列物质中,在一定条件下既能发生加成反应,也能发生取代反应,但不能使KMnO4酸性溶液褪色的是
| A.丙烯 | B.苯 | C.甲苯 | D.丙炔 |
由CH3CH3→CH3CH2Cl→CH2=CH2→CH3CH2OH的转化过程中的反应依次是
| A.取代消去加成 | B.裂解取代消去 |
| C.取代加成消去 | D.取代消去取代 |
已知某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法中不正确的是
| A.由红外光谱可知,该有机物中至少有三种不同的化学键 |
| B.由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子 |
| C.仅由其核磁共振氢谱无法得知其分子中的氢原子总数 |
| D.若A的化学式为C2H6O,则其结构简式为CH3—O—CH3 |